题目内容
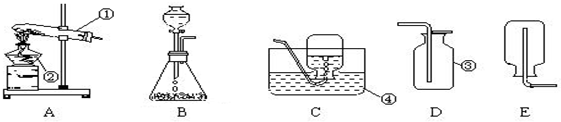
17. 从碳酸钠、氢氧化钠、稀盐酸、氯化钡、氯化钠几种溶液中取出其中的两种混合,回答下列问题:
从碳酸钠、氢氧化钠、稀盐酸、氯化钡、氯化钠几种溶液中取出其中的两种混合,回答下列问题:(1)能够发生反应的组合有3种.
(2)若混合后溶液质量减小,可能的组合是HCl、Na2CO3或Na2CO3、NaOH(任写一组组合).
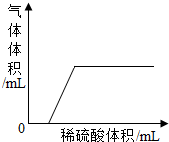
(3)将稀硫酸逐滴滴入剩下的几种组合中,若产生气体与加入稀硫酸有如图所示的关系,则这样的组合可能是NaOH、Na2CO3.
分析 理清复分解反应的条件:必须有水、沉淀或气体生成,两种溶液混合若有沉淀或气体生成,都会导致溶液质量减少;弄清图象表示的意义:刚开始时没有气泡生成,说明混合溶液中一定含有碱,而过一段时间后有气泡产生说明混合物中一定含有碳酸钠.
解答 解:(1)5种溶液两两混合,一共有10种组合,能发生反应的组合有:①氢氧化钠与稀盐酸;②碳酸钠与稀盐酸;③碳酸钠与氯化钡.
故答案是:3.
(2)混合后溶液质量减少,说明两种溶液混合反应生成了气体或沉淀,
故答案为:HCl、Na2CO3或Na2CO3、NaOH;
(2)根据图象不难看出有气泡冒出,那混合溶液中一定有碳酸钠,而刚开始时无气泡产生,说明混合溶液中有能够和酸反应但不能和碳酸钠反应的物质,因此另外一种物质是氢氧化钠而不是氢氧化钙,
故答案为:NaOH、Na2CO3.
点评 主要考查了复分解反应的条件,及根据反应的现象分析具体的反应情况,培养学生分析问题的能力.

练习册系列答案
相关题目
7.下列变化属于物理变化的是( )
| A. | 菜刀生锈 | B. | 牛奶变酸 | ||
| C. | 煤气泄漏遇火爆炸 | D. | 蒸汽锅炉爆炸 |
2.春天的校园花香四溢,该现象说明( )
| A. | 分子种类发生变化 | B. | 分子间的间隔变小 | ||
| C. | 分子的体积变大 | D. | 分子在不断运动 |
9.豆浆中含有异黄酮(C15H10O2)具有防癌功能.下列说法正确的是( )
| A. | 异黄酮中C、H元素的质量比为15:10 | B. | 异黄酮由C、H、O三种元素组成 | ||
| C. | 一个异黄酮分子中含有一个氧分子 | D. | 异黄酮由27个原子构成 |
6.下列元素对应的元素符号正确的是( )
| A. | 镁mg | B. | 氢He | C. | 铜Cn | D. | 铁Fe |