题目内容
10.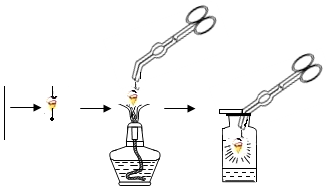 如图是铁丝在在氧气中燃烧的实验,请回答下列问题:
如图是铁丝在在氧气中燃烧的实验,请回答下列问题:(1)集气瓶底铺上一层细砂,其作用是防止生成物落下来炸裂集气瓶.
(2)该反应的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
分析 根据铁丝在氧气中燃烧实验注意事项分析有关问题;根据反应物、生成物及反应条件写出反应的化学方程式.
解答 解:(1)铁丝在氧气中燃烧时,为了防止溅落的熔化物炸裂集气瓶底,应在集气瓶底铺一层细砂;
(2)铁丝在氧气中燃烧生成了四氧化三铁,反应的方程式是:3Fe+2O2 $\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
故答案为:(1)防止生成物落下来炸裂集气瓶;(2)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
点评 本题主要考查铁燃烧的实验现象和化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.

练习册系列答案
相关题目
20.某校学习小组学习固体、液体的密度测量之后,准备探究气体密度的测定.学习小组认为气体密度的测定原理和小石块、盐水的密度测定一样.
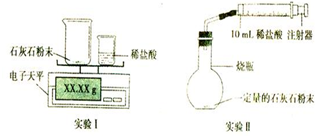
【提出问题】如何利用石灰石与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
【实验设计】通过下列两个实验分别测定CO2的质量和体积:
【分析与表达】
(1)实验I中,将小烧杯中的10ml稀盐酸加入到盛有石灰石的大烧杯中,并不断搅拌,直至不再产生气泡,发生反应的化学方程式为CaCO3+2HCl═CaCl2+CO2↑+H2O.
(2)实验II中,装好药品前先检查装置的气密性(填操作名称),然后,最后将10ml稀盐酸 快速推入烧瓶中.若稀盐酸是缓慢推入的,则可能造成的后果是烧瓶内气压增大,稀盐酸难以完全推入烧瓶中或仪器连接处脱落.
【记录与处理】
(3)实验产生的质量CO2为实验I中反应前的电子天平示数与完全反应后的示数差
(4)实验II的实验记录如表(表中数据在相同温度、相同压强条件下测定):
根据以上实验过程和数据综合分析,最终生成CO2的体积是80ml.
(5)根据(3)、(4)测得的数据,用密度的计算公式计算.
【实验反思】
(6)有同学认为实验I与II中盐酸以及石灰石的用量不仅要一样,而且石灰石要完全反应.
对于实验I与实验II中盐酸以及石灰石的用量要一样大家都赞同.但对于反应中应该石灰
石过量还是稀盐酸过量才不会影响实验结果有不同的看法,你的看法是:不管谁有剩余对实验结果都没有影响.

【提出问题】如何利用石灰石与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
【实验设计】通过下列两个实验分别测定CO2的质量和体积:
【分析与表达】
(1)实验I中,将小烧杯中的10ml稀盐酸加入到盛有石灰石的大烧杯中,并不断搅拌,直至不再产生气泡,发生反应的化学方程式为CaCO3+2HCl═CaCl2+CO2↑+H2O.
(2)实验II中,装好药品前先检查装置的气密性(填操作名称),然后,最后将10ml稀盐酸 快速推入烧瓶中.若稀盐酸是缓慢推入的,则可能造成的后果是烧瓶内气压增大,稀盐酸难以完全推入烧瓶中或仪器连接处脱落.
【记录与处理】
(3)实验产生的质量CO2为实验I中反应前的电子天平示数与完全反应后的示数差
(4)实验II的实验记录如表(表中数据在相同温度、相同压强条件下测定):
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/ml | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
(5)根据(3)、(4)测得的数据,用密度的计算公式计算.
【实验反思】
(6)有同学认为实验I与II中盐酸以及石灰石的用量不仅要一样,而且石灰石要完全反应.
对于实验I与实验II中盐酸以及石灰石的用量要一样大家都赞同.但对于反应中应该石灰
石过量还是稀盐酸过量才不会影响实验结果有不同的看法,你的看法是:不管谁有剩余对实验结果都没有影响.
15.生活中的铁锅、铝制易拉罐和铜线都属于( )
| A. | 金属材料 | B. | 化合物 | C. | 氧化物 | D. | 非金属材料 |
20.关于CO 的叙述不正确的是( )
| A. | CO 有可燃性和还原性 | |
| B. | CO 可用排水集气法收集 | |
| C. | CO 有毒,能跟血红蛋白结合,使人体缺氧 | |
| D. | CO 可用向上排空气法收集 |