题目内容
7.请你回答下列与金属有关的问题:(1)用序号回答:铝的利用比铜和铁晚得多,原因是②;在铁制品表面刷一层铝粉可以防止生锈,其主要原因是④.
①铝的硬度小 ②铝很活泼 ③地壳中铝的含量高 ④铝的表面易生成致密的保护膜
(2)为了防止月饼变质,常在月饼的内包装袋中放入一小包防腐剂,它的主要成分是铁粉,铁粉的作用是除去水和氧气,检验防腐剂中还含有铁粉的方法是取少量防腐剂于试管中,加入稀硫酸,有气泡产生.
(3)现提供下列实验药品:①Fe、Cu、Ag、稀硫酸;②FeSO4溶液、Cu、Ag;③Fe、Ag、CuSO4溶液,其中能验证Fe、Cu、Ag三种金属的活动顺序的是③(填序号),发生反应的化学方程式是Fe+CuSO4═Cu+FeSO4.
分析 在金属活动性顺序中,氢前的金属能与酸发生置换反应,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,铁在有水和氧气共存时易生锈.
解答 解:(1)在金属活动性顺序中,铝排在铜和铁的前面,性质活泼,铝在空气中表面容易与氧气反应生成致密的氧化物保护膜,所以本题答案为:②,④;
(2)铁在有水和氧气共存时易生锈,铁可以与酸反应生成氢气,所以本题答案为:除去水和氧气;取少量防腐剂于试管中,加入稀硫酸,有气泡产生;
(3)①铁能与硫酸反应生成氢气,而铜和银不可以,说明铁在铜和银的前面,不能说明铜和银的顺序,故①不对,②铜和银不能与硫酸亚铁反应,说明铜和银在铁的后面,不能说明铜和银的顺序,故②不对,③铁能将铜置换出来,说明铁在铜的前面,银不能与硫酸铜反应,说明铜在银的前面,故③正确,铁能与硫酸铜反应生成硫酸亚铁和铜,所以本题答案为:③,Fe+CuSO4═Cu+FeSO4.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.向100g质量分数为6%的氯化钠溶液中加入50g蒸馏水,所得溶液的溶质质量分数为( )
| A. | 4% | B. | 4.5% | C. | 3.8% | D. | 5% |
12.下列化学用语中,关于数字“2”的说法错误的是( )
①2H; ②SO2;③$\stackrel{+2}{Cu}$O; ④Mg2+.
①2H; ②SO2;③$\stackrel{+2}{Cu}$O; ④Mg2+.
| A. | 表示分子个数的是① | B. | 表示分子中原子个数的是② | ||
| C. | 表示元素化合价的是③ | D. | 表示离子所带电荷数的是④ |
16.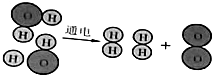 水通电分解的示意图,据图回答下列问题.
水通电分解的示意图,据图回答下列问题.
(1)通电前,两个水分子中共含有4个氢原子和2个氧原子,通电后有4个氢原子和2个氧原子.
(2)水通电分解过程中,原子的种类不变(填“改变”或“不变”,下同),各种原子的数目不变,而分子的种类改变.
(3)据图填写上表.
(4)由上表可知:任何一个化学反应都遵循质量守恒定律,不管反应物和生成物的质量是多少,各物质的质量比不变.
 水通电分解的示意图,据图回答下列问题.
水通电分解的示意图,据图回答下列问题.| 反应物 | 生成物 | ||
| H2O | O2 | ||
| A | 18g | 2g | |
| B | 8g | 64g | |
| 质量比 | |||
(2)水通电分解过程中,原子的种类不变(填“改变”或“不变”,下同),各种原子的数目不变,而分子的种类改变.
(3)据图填写上表.
(4)由上表可知:任何一个化学反应都遵循质量守恒定律,不管反应物和生成物的质量是多少,各物质的质量比不变.
 回答下列问题:
回答下列问题: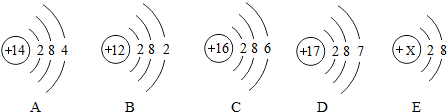
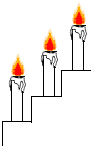 如图是三支高低不同的燃着的蜡烛,放在一只大的玻璃杯中,然后慢慢的往玻璃杯倒入二氧化碳气体,最先熄灭的是:下层的蜡烛,原因是二氧化碳的密度比空气大,而且不支持燃烧.
如图是三支高低不同的燃着的蜡烛,放在一只大的玻璃杯中,然后慢慢的往玻璃杯倒入二氧化碳气体,最先熄灭的是:下层的蜡烛,原因是二氧化碳的密度比空气大,而且不支持燃烧.