题目内容
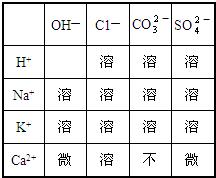
表列出了20℃时“部分酸、碱、盐的溶解性”.试回答下列问题:
(1)表中的离子相互结合,形成的盐酸盐有(填名称)
(2)用化学符号填空.碳酸钾溶液中存在的微粒有
(3)硫酸钠、硫酸钾的化学性质相似,是因为其溶液中都含有
(4)从表中选择离子组成两种化合物,它们之间能发生反应生成气体.反应的化学方程式为
| OH- | Cl- | CO32- | SO42- | |
| H+ | - | 溶 | 溶 | 溶 |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| K+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 不 | 微 |
氯化钠、氯化钾、氯化钙
氯化钠、氯化钾、氯化钙
;(2)用化学符号填空.碳酸钾溶液中存在的微粒有
K+ CO32-
K+ CO32-
;在碳酸钾与硫酸溶液的反应中,实质参加反应的离子是H+ CO32-
H+ CO32-
.(3)硫酸钠、硫酸钾的化学性质相似,是因为其溶液中都含有
SO42-
SO42-
.(4)从表中选择离子组成两种化合物,它们之间能发生反应生成气体.反应的化学方程式为
Na2CO3+2HCl═2NaCl+H2O+CO2↑(其它合理答案正确)
Na2CO3+2HCl═2NaCl+H2O+CO2↑(其它合理答案正确)
,反应类型属于复分解反应
复分解反应
.分析:(1)根据盐酸盐的组成特点解答
(2)根据物质溶于水的电离情况分析
(3)根据两种溶液组成上的相同点分析
(4)根据物质间反应规律分析
(2)根据物质溶于水的电离情况分析
(3)根据两种溶液组成上的相同点分析
(4)根据物质间反应规律分析
解答:解:(1)盐酸盐是氯离子和金属阳离子或铵根离子组成的,因此有氯化钠,氯化钾,氯化钙;
(2)碳酸钾溶液中存在钾离子和碳酸根离子,硫酸钾与硫酸溶液反应实质是碳酸根离子和氢离子结合成水和二氧化碳;
(3)硫酸钠、硫酸钾的溶液中都含有硫酸根离子,故化学性质相似
(4)盐酸与碳酸盐能反应生成 二氧化碳气体,化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑
该反应是两种化合物相互交换成分,生成另外两种化合物,属于复分解反应.
故答案为:(1)氯化钠、氯化钾、氯化钙;
(2)K+ CO32- H+ CO32-.
(3)SO42-.
(4)Na2CO3+2HCl═2NaCl+H2O+CO2↑(其它合理答案正确),复分解反应.
(2)碳酸钾溶液中存在钾离子和碳酸根离子,硫酸钾与硫酸溶液反应实质是碳酸根离子和氢离子结合成水和二氧化碳;
(3)硫酸钠、硫酸钾的溶液中都含有硫酸根离子,故化学性质相似
(4)盐酸与碳酸盐能反应生成 二氧化碳气体,化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑
该反应是两种化合物相互交换成分,生成另外两种化合物,属于复分解反应.
故答案为:(1)氯化钠、氯化钾、氯化钙;
(2)K+ CO32- H+ CO32-.
(3)SO42-.
(4)Na2CO3+2HCl═2NaCl+H2O+CO2↑(其它合理答案正确),复分解反应.
点评:学生应根据酸的概念来理解其溶液中的离子,利用复分解反应发生的条件来判断反应的发生并能书写相关的化学方程式.

练习册系列答案
相关题目
下表列出了20℃时“部分酸、碱、盐的溶解性”,试回答下列问题:
| OH― | C1― | CO | SO | |
| H+ | 溶 | 溶 | 溶 | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| K+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 不 | 微 |
(1)表中的离子相互结合,形成的酸有(填名称)________________________________;酸有相似的化学性质是因为酸溶液中都含有_________。
(2)用化学符号填空。氢氧化钾溶液中存在的微粒有__________________;在氢氧化钾与酸溶液的反应中,实质参加反应的离子是__________________。
(3)碳酸钠、碳酸钾的化学性质相似,是因为其溶液中都含有_________。氯化钠溶液与硫酸钾溶液能否发生反应? _________。理由是___________________________。
(4)从表中选择离子组成两种化合物,它们之间能发生反应生成气体。反应的化学方程式为__________________,反应类型属于_________。