题目内容
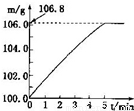
某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5g化肥样品与足量浓烧碱溶液加热,产生的氮气用100.0g废硫酸吸收.测得吸收氨气的溶液总质量m与反应时间t的变化如图所示,所涉及的反应为:(NH4)SO4+2NaOH=Na2SO4+2NH3+2H2O↑;2NH3+H2SO4=(NH4)SO4.请计算:(1)完全反应后产生氨气______g(2)该化肥的含氨量为______(精确到0.1%),则这种化肥属于______(填“合格”或“不合格”,合格硫酸铵含氮量为20%以上)产品.
(3)请计算废硫酸中硫酸的质量分数(写出计算过程)
【答案】分析:(1)运用质量守恒定律解答
(2)运用质量守恒定律和根据化学式的计算解答
(3)运用根据化学方程式的计算和溶液中溶质质量分数求解
解答:解:(1)根据质量守恒定律结合题中图示可知生成的氨气质量为106.8g-100g=6.8g,故(1)答案:6.8g
(2)根据质量守恒定律氨气中的氮元素质量即硫酸铵化肥中氮元素的质量,氨气中氮元素的质量为6.8g×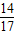 =5.6g,故化肥中氮元素的质量分数为
=5.6g,故化肥中氮元素的质量分数为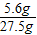 ×100%=20.4%
×100%=20.4%
设溶液中硫酸的质量为x
2NH3+H2SO4=(NH4)2SO4
34 98
6.8g x
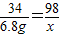
x=19.6g
废硫酸中硫酸的溶质质量分数为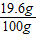 ×100%=19.6%
×100%=19.6%
答:溶液中硫酸的溶质质量分数为19.6%
故答案为:(1)6.8
(2)20.4% 合格
(3)19.6%
点评:本题是综合性计算题,考查质量守恒定律的计算、根据化学式的计算和溶质质量分数的计算,侧重计算能力的考查,平时学习时一定注意多做多总结规律,寻找解题思路.
(2)运用质量守恒定律和根据化学式的计算解答
(3)运用根据化学方程式的计算和溶液中溶质质量分数求解
解答:解:(1)根据质量守恒定律结合题中图示可知生成的氨气质量为106.8g-100g=6.8g,故(1)答案:6.8g
(2)根据质量守恒定律氨气中的氮元素质量即硫酸铵化肥中氮元素的质量,氨气中氮元素的质量为6.8g×
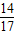 =5.6g,故化肥中氮元素的质量分数为
=5.6g,故化肥中氮元素的质量分数为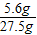 ×100%=20.4%
×100%=20.4%设溶液中硫酸的质量为x
2NH3+H2SO4=(NH4)2SO4
34 98
6.8g x
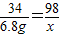
x=19.6g
废硫酸中硫酸的溶质质量分数为
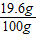 ×100%=19.6%
×100%=19.6%答:溶液中硫酸的溶质质量分数为19.6%
故答案为:(1)6.8
(2)20.4% 合格
(3)19.6%
点评:本题是综合性计算题,考查质量守恒定律的计算、根据化学式的计算和溶质质量分数的计算,侧重计算能力的考查,平时学习时一定注意多做多总结规律,寻找解题思路.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
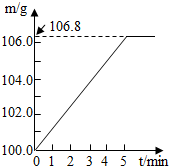 某同学为了检验家里购买的硫酸铵化肥是否合格,称取了27.5g化肥样品与足量浓烧碱溶液一起加热,产生的氨气用足量的100.0g废硫酸吸收.测得吸收氨气的溶液总质量m与反应时间t的变化如右图所示.已知合格硫酸铵化肥中含氮量不低.20%.所涉及的反应为(NH4)2SO4+2NaOH=Na2SO4+2H2O+2NH3↑;2NH3+H2SO4=(NH4)2SO4.试计算:
某同学为了检验家里购买的硫酸铵化肥是否合格,称取了27.5g化肥样品与足量浓烧碱溶液一起加热,产生的氨气用足量的100.0g废硫酸吸收.测得吸收氨气的溶液总质量m与反应时间t的变化如右图所示.已知合格硫酸铵化肥中含氮量不低.20%.所涉及的反应为(NH4)2SO4+2NaOH=Na2SO4+2H2O+2NH3↑;2NH3+H2SO4=(NH4)2SO4.试计算: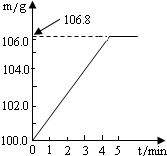
 (2011?和平区二模)某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5g化肥样品与足量浓烧碱溶液加热,产生的氮气用100.0g废硫酸吸收.测得吸收氨气的溶液总质量m与反应时间t的变化如图所示,所涉及的反应为:(NH4)SO4+2NaOH=Na2SO4+2NH3+2H2O↑;2NH3+H2SO4=(NH4)SO4.请计算:(1)完全反应后产生氨气
(2011?和平区二模)某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5g化肥样品与足量浓烧碱溶液加热,产生的氮气用100.0g废硫酸吸收.测得吸收氨气的溶液总质量m与反应时间t的变化如图所示,所涉及的反应为:(NH4)SO4+2NaOH=Na2SO4+2NH3+2H2O↑;2NH3+H2SO4=(NH4)SO4.请计算:(1)完全反应后产生氨气 某同学为了检验家里购买的硫酸铵化肥是否合格,称取了27.5g化肥样品与足量浓烧碱溶液一起加热,产生的氨气用足量的100.0g废硫酸吸收.测得吸收氨气的溶液总质量m与反应时间t的变化如右图所示.已知合格硫酸铵化肥中含氮量不低于20%.所涉及的反应为(NH4)2SO4+2NaOH=Na2SO4+2H2O+2NH3↑;2NH3+H2SO4=(NH4)2SO4.试计算:
某同学为了检验家里购买的硫酸铵化肥是否合格,称取了27.5g化肥样品与足量浓烧碱溶液一起加热,产生的氨气用足量的100.0g废硫酸吸收.测得吸收氨气的溶液总质量m与反应时间t的变化如右图所示.已知合格硫酸铵化肥中含氮量不低于20%.所涉及的反应为(NH4)2SO4+2NaOH=Na2SO4+2H2O+2NH3↑;2NH3+H2SO4=(NH4)2SO4.试计算: