题目内容
15.质量相等的两份氯酸钾①和②,向①中加入少量的二氧化锰,完全反应后,收集到氧气的质量随加热时间变化的函数图象正确的是( )| A. |  | B. |  | C. |  | D. |  |
分析 本题要从催化剂和反应条件角度考虑,氯酸钾在二氧化锰的催化作用下加热或加热到一定的温度都能产生氧气,质量相等的两份氯酸钾完全反应后收集到的氧气的量应该是相等的.
解答 解:相同质量的氯酸钾加热后生成氧气的质量是相同的;而加入二氧化锰的一份分解时需要的温度较低,最先分解,没有加入催化剂的一份需要的温度较高.
故选A.
点评 记住催化剂的“一改变,二不变”的特性,即“改变化学反应的速率;反应前后,自身的质量和化学性质都不改变”,另外,催化剂也不能改变生成物的质量.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目
3.如图是水通电分解的示意图,从中获得的信息不正确的是( )
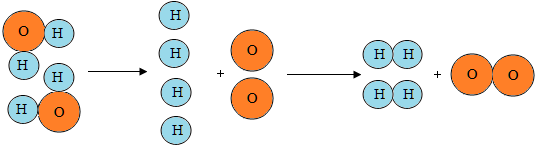
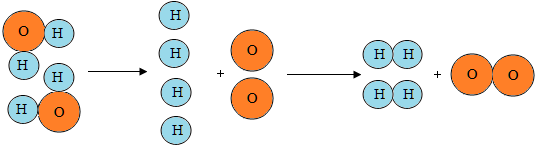
| A. | 原子是化学变化中的最小粒子 | |
| B. | 在一定条件下,水能分解生成氢气和氧气 | |
| C. | 在化学变化前后,分子和原子的种类都不变 | |
| D. | 在化学变化中,分子可以再分,原子不能再分 |
10.下列说法正确的是( )
| A. | 由两种物质生成一种物质的反应叫做化合反应 | |
| B. | 工业制氧气的方法是分离液态空气,为分解反应 | |
| C. | 石蜡的燃烧属于氧化反应,但不属于化合反应 | |
| D. | 在空气中不能燃烧的物质,在氧气中也不能燃烧 |
20.下列物质属于纯净物的是( )
| A. | 空气 | B. | 蒸馏水 | C. | 75%的医用酒精 | D. | 蔗糖水 |
7.化学源于生活,生活中的下列做法不正确的是( )
| A. | 用稀盐酸可以除水垢 | B. | 炒菜时油锅起火用锅盖盖灭 | ||
| C. | 在篮球架的表面喷漆防锈 | D. | 用吸附的方法使硬水软化 |
4.医用生理盐水是0.9% 的NaCl溶液,下列有关说法中,错误的是( )
| A. | 属于混合物 | B. | 溶质是氯化钠 | C. | 用前要摇匀 | D. | 静置时不分层 |
5.在物质混合、反应等过程中,会存在“1+1≠2”的现象.通常情况下,下列各种混合或反应过程中,“1+1”不等于“2”的是( )
| A. | 1g酒精和1g水混合后的总质量 | |
| B. | 1g金属锌和1g稀盐酸反应后溶液的质量 | |
| C. | 温度一定时1g不饱和硝酸钾溶液中加入1g硝酸钾后,所得溶液的质量 | |
| D. | 1g氢氧化钠溶液和1g醋酸溶液混合后溶液的质量 |