题目内容
14.已知钠、钾等金属在常温下可与水发生剧烈反应生成氢气,如金属钠与水的反应方程式为:2Na+2H2O═2NaOH+H2↑,据此判断下列说法中不正确的是( )| A. | 钠的化学性质比铁活泼 | B. | 该反应的基本类型为置换反应 | ||
| C. | 反应后的溶液显碱性 | D. | 参加反应的钠与水的质量比为1:1 |
分析 根据提供的信息可以判断相关方面的问题.
解答 解:A、通常情况下,铁不能和水反应,钠能和水反应,说明钠的化学性质比铁活泼,该选项说法正确;
B、2Na+2H2O═2NaOH+H2↑中,反应物和生成物都是一种单质和一种化合物,属于置换反应,该选项说法正确;
C、反应后得到氢氧化钠溶液,氢氧化钠属于碱,因此氢氧化钠溶液显碱性,该选项说法正确;
D、反应物和生成物之间的质量关系为:2Na+2H2O═2NaOH+H2↑,
46 36 80 2
参加反应的钠与水的质量比为:46:36=23:18,该选项说法不正确.
故选:D.
点评 根据金属与水反应的难易程度可以判断金属之间的活泼性,要注意理解.

练习册系列答案
 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
4.生活中,下列物质的用途与化学性质无关的是( )
| A. | 用氮气保存食品 | B. | 用擦酒精的方法给发热病人降温 | ||
| C. | 用焦炭冶炼金属 | D. | 用小苏打蒸馒头 |
5.下列说法正确的是( )
| A. | 饱和氯化钠溶液中加入硝酸钾,氯化钠质量分数不变 | |
| B. | 气体的溶解度与温度、压强、水的用量都有关 | |
| C. | 硝酸钾溶液降温析出晶体后变为不饱和溶液 | |
| D. | 汽油作溶剂可以除去油污 |
9.一种固体物质受热变成气体,下列关于此变化判断正确的是( )
| A. | 一定放出热量 | B. | 不可能是分解反应 | ||
| C. | 一定是化学变化 | D. | 可能是物理变化 |
19. 某化学兴趣小组同学用实验室中的过氧化钠(Na2O2)粉末进行实验,取少量粉末放入试管中并加入水,观察到有气泡产生,用带火星的木条放在试管口,木条复燃,则该气体是氧气;另取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红.
某化学兴趣小组同学用实验室中的过氧化钠(Na2O2)粉末进行实验,取少量粉末放入试管中并加入水,观察到有气泡产生,用带火星的木条放在试管口,木条复燃,则该气体是氧气;另取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红.
【提出问题】溶液为什么会变红呢?
【查阅资料】过氧化钠与水发生了化学反应,生成碱性物质,碱性物质能使酚酞试液变红.
【猜想假设】甲同学认为生成了碳酸钠; 乙同学认为生成了氢氧化钠.
【实验探究】
(1)小明认为甲同学的猜想无需验证就知道是错误的.他的理由是反应物中不含有碳元素,因此不能生成碳酸钠.
(2)为了证实小明的看法,小组设计了一个证明碳酸钠不存在并验证生成物的实验.
【得出结论】根据实验分析,过氧化钠与水反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑.
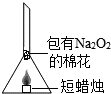
【拓展反思】过氧化钠不仅可以和水发生反应,也可以和二氧化碳反应生成氧气.小红同学又设计了一个如图所示实验(蜡烛火焰与棉花不接触).请回答:
(1)棉花能(填“能”或“不能”)燃烧,这主要是因为蜡烛燃烧生成了能与过氧化钠反应的物质水和二氧化碳,同时反应放热.
(2)结合上述实验事实,请你对运输过氧化钠固体过程中提出一条安全建议:密封保存.
 某化学兴趣小组同学用实验室中的过氧化钠(Na2O2)粉末进行实验,取少量粉末放入试管中并加入水,观察到有气泡产生,用带火星的木条放在试管口,木条复燃,则该气体是氧气;另取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红.
某化学兴趣小组同学用实验室中的过氧化钠(Na2O2)粉末进行实验,取少量粉末放入试管中并加入水,观察到有气泡产生,用带火星的木条放在试管口,木条复燃,则该气体是氧气;另取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红.【提出问题】溶液为什么会变红呢?
【查阅资料】过氧化钠与水发生了化学反应,生成碱性物质,碱性物质能使酚酞试液变红.
【猜想假设】甲同学认为生成了碳酸钠; 乙同学认为生成了氢氧化钠.
【实验探究】
(1)小明认为甲同学的猜想无需验证就知道是错误的.他的理由是反应物中不含有碳元素,因此不能生成碳酸钠.
(2)为了证实小明的看法,小组设计了一个证明碳酸钠不存在并验证生成物的实验.
| 实验操作 | 实验现象 | 实验结论 |
| 取过氧化钠与水反应后的溶液放入试管中,向其中滴加足量稀盐酸. | 无气泡产生 | 不存在碳酸钠 |
| 另取过氧化钠与水反应后的溶液放入试管中,向其中滴加硫酸铜溶液. | 产生蓝色沉淀 | 乙猜想正确 |
【拓展反思】过氧化钠不仅可以和水发生反应,也可以和二氧化碳反应生成氧气.小红同学又设计了一个如图所示实验(蜡烛火焰与棉花不接触).请回答:
(1)棉花能(填“能”或“不能”)燃烧,这主要是因为蜡烛燃烧生成了能与过氧化钠反应的物质水和二氧化碳,同时反应放热.
(2)结合上述实验事实,请你对运输过氧化钠固体过程中提出一条安全建议:密封保存.
6.新型净水剂高铁酸钾(K2FeO4)中铁元素的化合价为( )
| A. | +2 | B. | +3 | C. | +6 | D. | +7 |
3.下列实验操作正确的是( )
| A. |  给液体加热 | B. |  倾倒液体 | C. |  称量固体 | D. |  氧气验满 |
4.下列关于实验现象的描述正确的是( )
| A. | 铁丝在氧气中燃烧生成四氧化三铁 | |
| B. | 二氧化碳通入紫色石蕊溶液中,溶液变为蓝色 | |
| C. | 电解水实验中,正极端与负极端产生的气体体积比约为1:2 | |
| D. | 氢气在空气中燃烧产生黄色火焰 |