题目内容
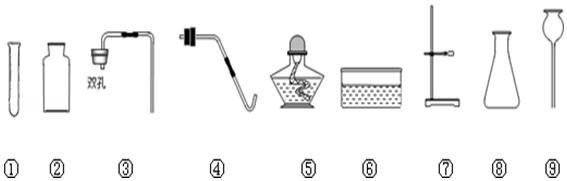
9.如图所示为实验室常用的实验装置,据此回答下列问题:
(1)写出标号仪器的名称:a长颈漏斗,b锥形瓶
(2)实验室用A装置制取氧气的化学方程式为2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;若从氯酸钾和二氧化锰混合物制取O2后的固体残渣中回收二氧化锰,可通过以下四步实验进行回收,则正确的操作顺序是bcda(填序号).
a、烘干 b、溶解 c、过滤 d、洗涤
(3)制取二氧化碳气体选择发生装置为B(填序号),反应方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;氧气和二氧化碳都可以用C装置(填序号)来收集.
分析 (1)熟记仪器的名称;
(2)根据气体的制取装置确定反应的原理,结合分离混合物的方法来解答;
(3)根据反应物的状态与反应的条件确定制取装置,根据化学反应的原理书写化学方程式,根据气体的密度与溶解性确定收集方法.
解答 解:(1)仪器a是长颈漏斗,b是锥形瓶;故填:长颈漏斗;锥形瓶;
(2)装置A适用于固体加热制取氧气,因为试管口没有棉花团,所以是加热氯酸钾与二氧化锰的混合物制取氧气,同时生成氯化钾,生成的氯化钾能溶于水,而二氧化锰难溶于水,所以从氯酸钾和二氧化锰混合物制取O2后的固体残渣中回收二氧化锰,可以采取溶解、过滤、洗涤、干燥的方法;故填:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;bcda;
(3)实验室通常用大理石或石灰石与稀盐酸反应制取二氧化碳,属于固液常温型,所以选择装置B来制取,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;氧气的密度比空气大,不易溶于水,二氧化碳的密度比空气大,能溶于水,所以二者均可用向上排空气法来收集;故填:B;CaCO3+2HCl=CaCl2+H2O+CO2↑;C.
点评 本题主要考查仪器的用途、反应表达式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.

练习册系列答案
 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
10.下列对某一主题的知识归纳,有错误的一组是( )
| A物质鉴别 | 硫酸钾和硫酸铵--熟石灰混合研磨,闻气味 |
| 羊毛纤维与合成纤维--灼烧、闻气味 | |
| B物质除杂 | 盐酸中混有硫酸--加适量氯化钡溶液过滤 |
| 木炭粉中混有铁粉--磁铁吸引 | |
| C安全知识 | 电器着火--切断电源,再用干粉灭火器灭火 |
| 不慎将浓硫酸沾到皮肤或衣服上,应立即用大量水冲洗 | |
| D物质与微粒构成 | 水--由氢原子和氧原子构成 |
| 氯化钠--由钠离子和氯离子构成 |
| A. | A | B. | B | C. | C | D. | D |
7.宏观和微观相结合是认识物质结构的有效方法之一.
(1)已知:X、Y、Z、W四种粒子的核电荷数及核外各电子层电子排布情况如下表.
请回答下列问题:
①若X表示原子,a=6.单质X2与单质Z的反应中,X原子得到(填“得到”或“失去”)电子.
②Y、W形成的化合物化学式为MgCl2(用元素符号表示).
(2)将稀硫酸与烧杯中Fe、Cu两种金属相混合,微观变化情况如下图:

未参加反应的金属:Cu,烧杯中发生反应的化学方程式:Fe+H2SO4═FeSO4+H2↑.
(1)已知:X、Y、Z、W四种粒子的核电荷数及核外各电子层电子排布情况如下表.
| X | Y | Z | W | ||
| 对应元素名称 | 氧 | 镁 | 铝 | 氯 | |
| 核电荷数 | 8 | 12 | 13 | 17 | |
| 电子层 | 第一层 | 2 | 2 | 2 | 2 |
| 第二层 | a | 8 | 8 | 8 | |
| 第三层 | 3 | 8 | |||
①若X表示原子,a=6.单质X2与单质Z的反应中,X原子得到(填“得到”或“失去”)电子.
②Y、W形成的化合物化学式为MgCl2(用元素符号表示).
(2)将稀硫酸与烧杯中Fe、Cu两种金属相混合,微观变化情况如下图:

未参加反应的金属:Cu,烧杯中发生反应的化学方程式:Fe+H2SO4═FeSO4+H2↑.
4.同学们一起探究铝、铁、铜三种金属的活动性,小刚同学设计了用铜丝、铁丝、铝丝和稀盐酸,只用一只试管,取一次盐酸的探究方案.请你和他们一起完善下表的探究方案并回答有关问题.
(1)填写表格:
结论:金属活动性Al>Fe>Cu
(2)写出此实验中发生反应的两条化学方程式:Fe+2HCl═FeCl2+H2↑.2Al+3FeCl2=2AlCl3+3Fe.
(3)小华同学认为在小刚设计的方案中,只要补充一个实验,就可得出Al>Fe>H>Cu的结论.小华要补充的实验是把铜丝插入稀盐酸中.
(1)填写表格:
| 实验步骤 | 观察到的现象 |
| ①在试管中取少量盐酸,插入铁丝,充分作用. | 产生气泡,溶液变浅绿色 |
| ②在①所得的溶液中,插入铜丝,充分作用. | 无明显现象 |
| ③在②所得的溶液中插入铝丝,充分作用. | 铝丝表面会覆盖一层黑色物质,溶液变为无色 |
(2)写出此实验中发生反应的两条化学方程式:Fe+2HCl═FeCl2+H2↑.2Al+3FeCl2=2AlCl3+3Fe.
(3)小华同学认为在小刚设计的方案中,只要补充一个实验,就可得出Al>Fe>H>Cu的结论.小华要补充的实验是把铜丝插入稀盐酸中.
1.下列符号中,既能表示一个原子,又能表示一种元素,还能表示一种物质的是( )
| A. | 2O | B. | H2 | C. | He | D. | Cl |
 将等质量锌粉和铁粉,分别放入相同的足量稀盐酸中,反应后生成氢气质量与反应时间(t)的关系如图所示,据图回答:
将等质量锌粉和铁粉,分别放入相同的足量稀盐酸中,反应后生成氢气质量与反应时间(t)的关系如图所示,据图回答: