题目内容
2.从公元1世纪起,铁便成了我国最主要的金属.下列有关铁的叙述,正确的是( )| A. | 纯铁具有明亮的红色金属光泽 | B. | 铁具有导电和导热的性质 | ||
| C. | 铁是地壳中含量最多的金属元素 | D. | 铁在氧气中燃烧生成黑色的氧化铁 |
分析 纯净的铁是一种银白色金属;
铁具有良好的导电性和导热性;
铝是地壳中含量最多的金属元素;
铁在氧气中燃烧生成四氧化三铁.
解答 解:A、纯铁具有明亮的银白色金属光泽,该选项说法不正确;
B、铁具有导电和导热的性质,该选项说法正确;
C、铁不是地壳中含量最多的金属元素,该选项说法不正确;
D、铁在氧气中燃烧生成黑色的四氧化三铁,该选项说法不正确.
故选:B.
点评 纯净的铁比较软,而铁的合金硬度大,机械性能优良,因此生活、生产中经常用的是铁的合金.

练习册系列答案
相关题目
12.下列叙述正确的是( )
| A. | 温度计中的水银受热体积膨胀,因为汞原子受热体积变大 | |
| B. | 二氧化碳是由一个碳元素和二个氧元素组成的 | |
| C. | 水分子是由氢分子和氧原子构成的 | |
| D. | 五氧化二磷是由磷元素和氧元素组成的 |
14.下列叙述正确的是( )
| A. | 4 g氢气和8 g氧气混合,点燃充分反应生成12 g水 | |
| B. | 3 g木炭在空气中完全燃烧,生成11 g二氧化碳,参加反应的氧气的质量为8 g | |
| C. | 蜡烛燃烧后,蜡烛与氧气的质量总和与生成的气体的质量相等 | |
| D. | 镁条在空气里燃烧,生成的氧化镁的质量一定大于镁条的 |
11.为研究锌和铝的金属活动性,某研究小组进行了如下探究.
(1)小明设计的实验方案:向表面积相同的铝片和锌粒中分别加入盐酸.写出锌与盐酸反应的化学方程式Zn+2HCl═ZnCl2+H2↑.
(2)小芳将去膜和未去膜的铝片分别放入盐酸中,发现前者反应比后者快,原因是未去膜的铝片表面有氧化铝(氧化膜),氧化铝先与盐酸反应.
(3)小芳在(2)实验中,还观察到都有“灰黑色沉淀”这一异常现象出现.
【提出问题】铝与盐酸反应出现的灰黑色沉淀的组成是什么?
【查阅资料】铝在颗粒较小时为灰黑色;AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇.
【提出合理假设】假设a:灰黑色沉淀可能含有铝(或铝和氯化铝的混合物);
假设b:灰黑色沉淀可能含有AlCl3
假设c:灰黑色沉淀可能含有难溶于酸的物质.
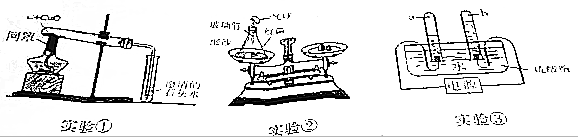
【设计并完成实验】取灰黑色沉淀分别做如下实验.
【得出结论】由实验①可判断假设c不成立(填“成立”或“不成立”),再结合实验②和③可得出该灰黑色沉淀的成分是铝和氯化铝.
(4)你认为(1)中小明的实验能否比较锌和铝的金属活动性强弱?不能(填“能”或“不能”).
(1)小明设计的实验方案:向表面积相同的铝片和锌粒中分别加入盐酸.写出锌与盐酸反应的化学方程式Zn+2HCl═ZnCl2+H2↑.
(2)小芳将去膜和未去膜的铝片分别放入盐酸中,发现前者反应比后者快,原因是未去膜的铝片表面有氧化铝(氧化膜),氧化铝先与盐酸反应.
(3)小芳在(2)实验中,还观察到都有“灰黑色沉淀”这一异常现象出现.
【提出问题】铝与盐酸反应出现的灰黑色沉淀的组成是什么?
【查阅资料】铝在颗粒较小时为灰黑色;AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇.
【提出合理假设】假设a:灰黑色沉淀可能含有铝(或铝和氯化铝的混合物);
假设b:灰黑色沉淀可能含有AlCl3
假设c:灰黑色沉淀可能含有难溶于酸的物质.
【设计并完成实验】取灰黑色沉淀分别做如下实验.
| 实验编号 | 实验操作 | 实验现象 |
| ① | 加入适量稀硫酸 | 有微量气泡,固体全部溶解,得到无色澄清溶液 |
| ② | 加入适量蒸馏水 | 固体部分溶解 |
| ③ | 加入适量无水乙醇 | 固体部分溶解 |
(4)你认为(1)中小明的实验能否比较锌和铝的金属活动性强弱?不能(填“能”或“不能”).