题目内容
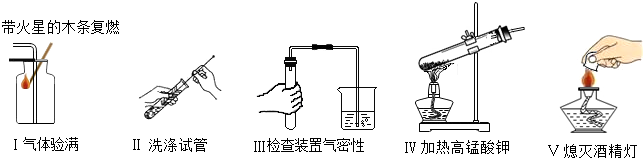
实验室开放日,某化学兴趣小组的同学在老师的指导下,设计了如图1实验装置进行气体制取和性质的探究,请回答有关问题:
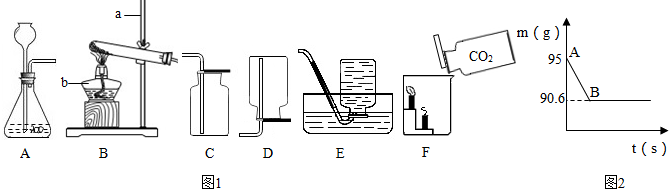
(1)请写出图中标有字母的仪器名称:a b
(2)实验室用氯酸钾和二氧化锰混合制取氧气时,应选用的发生装置是 (填写装置的字母代号,下同),请写出该反应的化学方程式: ,其中二氧化锰起 作用.
(3)实验室制取二氧化碳气体时,应选择的发生装置和收集装置是 .请写出用澄清石灰水检验二氧化碳时发生反应的化学方程式: .
(4)如图F所示,向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳具有的性质是 .
(5)鸡蛋壳的主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图2所示(忽略水蒸气的挥发),试计算(计算结果保留1位小数):
①产生CO2的质量
②该鸡蛋壳中CaCO3的质量分数.

(1)请写出图中标有字母的仪器名称:a
(2)实验室用氯酸钾和二氧化锰混合制取氧气时,应选用的发生装置是
(3)实验室制取二氧化碳气体时,应选择的发生装置和收集装置是
(4)如图F所示,向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳具有的性质是
(5)鸡蛋壳的主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图2所示(忽略水蒸气的挥发),试计算(计算结果保留1位小数):
①产生CO2的质量
②该鸡蛋壳中CaCO3的质量分数.
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,二氧化碳的实验室制法,二氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)根据常用仪器回答;
(2)根据实验室制取氧气的反应物的状态和反应条件选择发生装置,据反应原理书写方程式,二氧化锰是反应的催化剂;
(3)据实验室制取二氧化碳的反应原理及二氧化碳的性质分析选择发生和收集装置,检验二氧化碳用澄清的石灰水,据二氧化碳和氢氧化钙反应原理书写方程式;
(4)根据实验现象分析实验结论;
(5)①碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,生成的二氧化碳扩散到空气中,烧杯中前后减少的质量即为二氧化碳的质量;
②根据二氧化碳的质量求出碳酸钙的质量,再根据
×100%求出鸡蛋壳中碳酸钙的质量分数.
(2)根据实验室制取氧气的反应物的状态和反应条件选择发生装置,据反应原理书写方程式,二氧化锰是反应的催化剂;
(3)据实验室制取二氧化碳的反应原理及二氧化碳的性质分析选择发生和收集装置,检验二氧化碳用澄清的石灰水,据二氧化碳和氢氧化钙反应原理书写方程式;
(4)根据实验现象分析实验结论;
(5)①碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,生成的二氧化碳扩散到空气中,烧杯中前后减少的质量即为二氧化碳的质量;
②根据二氧化碳的质量求出碳酸钙的质量,再根据
| 碳酸钙的质量 |
| 鸡蛋壳的质量 |
解答:解:(1)标号仪器分别是铁架台和酒精灯;
(2)实验室用氯酸钾和二氧化锰混合制取氧气属于固体加热型,故选发生装置B,氯酸钾在二氧化锰的催化作用、加热的条件下生成氯化钾和氧气,反应方程式是:2KClO3
2KCl+3O2↑,二氧化锰是反应的催化剂;
(3)实验室制取二氧化碳用大理石和稀盐酸常温反应制取,属于固液常温型,故选发生装置A,二氧化碳的密度比空气大且能溶于水,故用向上排空气法收集;检验二氧化碳用澄清的石灰水,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,方程式是:CO2+Ca(OH)2═CaCO3↓+H2O;
(4)向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳密度比空气大,不能燃烧且不能支持燃烧;
产生CO2的质量为:95g-90.6g=4.4g 故答案为:4.4g
(5)①据质量守恒定律反应减少的质量就是二氧化碳的质量,产生CO2的质量为:95g-90.6g=4.4g;
②设鸡蛋壳中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
=
x=10g
×100%=66.7%
故答案为:(1)铁架台;酒精灯;
(2)B;2KClO3
2KCl+3O2↑;催化;
(3)AC;CO2+Ca(OH)2═CaCO3↓+H2O;
(4)二氧化碳密度比空气大,不能燃烧且不能支持燃烧;
(5)①4.4g;②鸡蛋壳中碳酸钙的质量分数为66.7%.
(2)实验室用氯酸钾和二氧化锰混合制取氧气属于固体加热型,故选发生装置B,氯酸钾在二氧化锰的催化作用、加热的条件下生成氯化钾和氧气,反应方程式是:2KClO3
| ||
| △ |
(3)实验室制取二氧化碳用大理石和稀盐酸常温反应制取,属于固液常温型,故选发生装置A,二氧化碳的密度比空气大且能溶于水,故用向上排空气法收集;检验二氧化碳用澄清的石灰水,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,方程式是:CO2+Ca(OH)2═CaCO3↓+H2O;
(4)向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳密度比空气大,不能燃烧且不能支持燃烧;
产生CO2的质量为:95g-90.6g=4.4g 故答案为:4.4g
(5)①据质量守恒定律反应减少的质量就是二氧化碳的质量,产生CO2的质量为:95g-90.6g=4.4g;
②设鸡蛋壳中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
| 100 |
| x |
| 44 |
| 4.4g |
x=10g
| 10g |
| 15g |
故答案为:(1)铁架台;酒精灯;
(2)B;2KClO3
| ||
| △ |
(3)AC;CO2+Ca(OH)2═CaCO3↓+H2O;
(4)二氧化碳密度比空气大,不能燃烧且不能支持燃烧;
(5)①4.4g;②鸡蛋壳中碳酸钙的质量分数为66.7%.
点评:本题考查知识较为综合,既考查了发生和收集装置的选取、反应原理等知识,又考查了据方程式的计算,能很好的考查学生分析、解决问题的能力.

练习册系列答案
相关题目
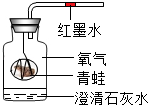 (1)现有空气、氧气、二氧化碳三种无色气体,请你从中任选二种气体,并用两种不同的方法鉴别它们.
(1)现有空气、氧气、二氧化碳三种无色气体,请你从中任选二种气体,并用两种不同的方法鉴别它们.