题目内容
3.小明同学在课外阅读中得知:钠是一种活泼金属,常温下能与氧气,水发生反应,其中钠与水反应的化学方程式为:2Na+2H2O═2NaOH+H2↑,在实验室,该同学选取50ml一定溶质质量分数的硫酸铜溶液于烧杯中,再取绿豆大小的钠投入硫酸铜溶液中,充分反应后过滤,得到滤液和蓝色滤渣,并对滤液的成分进行探究.【提出问题】滤液中溶质的成分是什么?
【查阅资料】已知Na2SO4的水溶液呈中性.
【猜想与假设】
猜想一:Na2SO4;
猜想二:Na2SO4、NaOH;
猜想三:Na2SO4、CuSO4;
猜想四:Na2SO4、CuSO4、NaOH;
其中不合理的是硫酸铜与氢氧化钠不能在溶液中共存;
【实验方案与验证】
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| 实验一 | 取少量滤液于试管中,观察现象 | 溶液为无色 | 猜想一或二成立 |
| 实验二 | 另取少量滤液于试管中,向其中滴加酚酞试剂 | 无明显现象 | 猜想一成立 |
| 实验三 | 常温下,再取少量滤液,测溶液酸碱度 | pH=7 | 猜想一成立 |
分析 【猜想与假设】根据反应物有可能剩余来分析;
【实验方案与验证】实验一:根据硫酸铜溶液是蓝色的来分析;
实验二:根据氢氧化钠溶液显碱性来分析;
实验三:根据溶液的酸碱性来分析;
【拓展延伸】根据题干信息来分析.
解答 解:【猜想与假设】将金属钠投入硫酸铜溶液中后,钠与水反应生成氢氧化钠与氢气,氢氧化钠与硫酸铜反应生成氢氧化铜蓝色沉淀和硫酸钠.
若氢氧化钠与硫酸铜恰好完全反应,二者都没有剩余则反应后的溶液中溶质只有硫酸钠.
若氢氧化钠有剩余,则反应后的溶液中溶质有硫酸钠、氢氧化钠;
所以硫酸铜有剩余,反应后的溶液中溶质有硫酸钠、硫酸铜.
因为硫酸铜与氢氧化钠能发生复分解反应,所以二者不能共存.
故填:Na2SO4、NaOH;硫酸铜与氢氧化钠不能在溶液中共存(答案合理即可);
【实验方案与验证】
实验一:因为硫酸铜溶液是蓝色,所以若滤液为无色,则一定不含硫酸铜,即猜想一或猜想二成立;故填:一或二;
实验二:氢氧化钠溶液显碱性,能使无色的酚酞试液变红色,而该滤液不能使之变色,所以滤液中一定不含氢氧化钠,所以猜想一成立;故填:一;
实验三:氢氧化钠溶液显碱性,pH>7;Na2SO4的水溶液呈中性,pH=7,所以若滤液的pH=7,则猜想一成立;故填:一;
【拓展延伸】因为金属钠的化学性质活泼,且能与水反应,所以要防潮.故填:防潮.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
13. 知识梳理有助于我们对已学知识的巩固,在学习物质结构层次后,某同学以氧气为例进行如图梳理,下列选项中与a、b、c相对应的是( )
知识梳理有助于我们对已学知识的巩固,在学习物质结构层次后,某同学以氧气为例进行如图梳理,下列选项中与a、b、c相对应的是( )
 知识梳理有助于我们对已学知识的巩固,在学习物质结构层次后,某同学以氧气为例进行如图梳理,下列选项中与a、b、c相对应的是( )
知识梳理有助于我们对已学知识的巩固,在学习物质结构层次后,某同学以氧气为例进行如图梳理,下列选项中与a、b、c相对应的是( )| A. | 原子、原子核、核外电子 | B. | 原子核、原子、核外电子 | ||
| C. | 原子、核外电子、原子核 | D. | 核外电子、原子核、原子 |
14. 如图为M、N两种固体饱和溶液中溶质的质量分数(C%)随温度(t)变化的曲线,下列说法中正确的是( )
如图为M、N两种固体饱和溶液中溶质的质量分数(C%)随温度(t)变化的曲线,下列说法中正确的是( )
 如图为M、N两种固体饱和溶液中溶质的质量分数(C%)随温度(t)变化的曲线,下列说法中正确的是( )
如图为M、N两种固体饱和溶液中溶质的质量分数(C%)随温度(t)变化的曲线,下列说法中正确的是( )| A. | 50 g M放入150 g水中形成不饱和溶液 | |
| B. | t1℃时,M的饱和溶液中溶质与溶剂的质量比为2:5 | |
| C. | 80 g N放入150 g水中全部溶解,溶液的温度一定低于t1℃ | |
| D. | 100 g N的溶液,蒸发15 g水、冷却至t1℃后析出10 g晶体,原溶液中溶质的质量分数为40% |
15. 元素周期表是学习化学的重要工具,如图是元素周期表中的一格,下面从该图获取的信息中,正确的是( )
元素周期表是学习化学的重要工具,如图是元素周期表中的一格,下面从该图获取的信息中,正确的是( )
 元素周期表是学习化学的重要工具,如图是元素周期表中的一格,下面从该图获取的信息中,正确的是( )
元素周期表是学习化学的重要工具,如图是元素周期表中的一格,下面从该图获取的信息中,正确的是( )| A. | 该元素相对原子质量为52kg | B. | 该元素属于非金属元素 | ||
| C. | 该元素的核外有24个电子 | D. | 该元素的原子序数为52 |
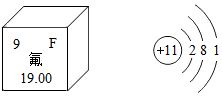 氟化钠是某些牙膏的添加剂,能有效预防龋齿,如图是氟元素在元素周期表中的相关信息及钠原子结构示意图,则氟原子的核外电子数是9,钠原子在化学反应中易失(填“得”或“失”)电子,氟化钠可以用钠与氟气(F2)反应制得,反应的化学方程式是2Na+F2═2NaF.
氟化钠是某些牙膏的添加剂,能有效预防龋齿,如图是氟元素在元素周期表中的相关信息及钠原子结构示意图,则氟原子的核外电子数是9,钠原子在化学反应中易失(填“得”或“失”)电子,氟化钠可以用钠与氟气(F2)反应制得,反应的化学方程式是2Na+F2═2NaF.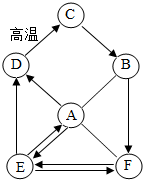 A、B、C、D、E、F之间存在如图的转化关系(部分物质及反应条件已略去),已知A是一种气体肥料;D含有人体中含量最高的金属元素,其相对分子质量为100.则D的化学式为CaCO3;E→F的化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;图示转化关系中未涉及到的基本反应类型是置换反应.
A、B、C、D、E、F之间存在如图的转化关系(部分物质及反应条件已略去),已知A是一种气体肥料;D含有人体中含量最高的金属元素,其相对分子质量为100.则D的化学式为CaCO3;E→F的化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;图示转化关系中未涉及到的基本反应类型是置换反应.