题目内容
10.在过氧化氢溶液的分解反应中,二氧化锰能作催化剂.下列有关催化剂的说法正确的是D(选填序号).A.在化学反应后其质量减小 B.在化学反应后其化学性质发生了变化
C.能增大生成物的质量 D.能改变化学反应速率
【提出问题】在过氧化氢溶液的分解反应中,除了二氧化锰,是否有其他物质也能作催化剂?
【查阅资料】在过氧化氢溶液的分解反应中,氧化铜也能作催化剂.
【进行实验】用天平称量0.2g氧化铜,取5mL5%过氧化氢溶液于试管中,进行如下实验:
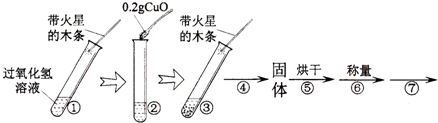
(1)填写表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦操作 | 结论 |
| 剧烈反应,有气泡产生,带火星的木条复燃 | 称量的氧化铜的质量仍为0.2g | 重复步骤溶液中有气泡放出,带火星的木条复燃 | 在过氧化氢溶液的分解反应中,氧化铜也能作催化剂 |
分析 根据催化剂的特点:催化剂只改变反应速率,但本身的质量和化学性质不变进行解答;
【实验】(1)根据氧化铜对过氧化氢的分解有催化作用回答③现象;根据催化剂的定义和特点回答⑥结果;根据催化剂的定义和特点回答⑦现象.
(2)根据对比实验的探究方法回答.
解答 解:催化剂只改变反应速率,但本身的质量和化学性质不变,可知
A.在化学反应后其质量不变,故错误;
B.在化学反应后其化学性质不变,故错误;
C.不影响生成物的质量,故错误;
D.能改变化学反应速率,故正确;
故选:D;
【实验】(1)氧化铜对过氧化氢的分解有催化作用,能加快其分解速率生成氧气的速率,故步骤③中的现象是有气泡产生,带火星的木条复燃;催化剂的特点是“一变,两不变”,反应前后其质量不变,所以步骤⑥中称量的氧化铜的质量仍为0.2g;催化剂的特点是“一变,两不变”,其中反应速率改变,这里是加快,所以⑦的现象是溶液中有气泡放出,带火星的木条复燃;
(2)为了看氧化铜是否能改变反应的速率,要通过加入氧化铜与不加氧化铜的现象进行对比,才能得出科学合理的结论.
故答案为:D;
(1)
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 剧烈反应,有气泡产生,带火星的木条复燃 | 称量的氧化铜的质量仍为0.2g | 溶液中有气泡放出;带火星的木条复燃 | 在过氧化氢溶液的分解反应中,氧化铜也能作催化剂 |
点评 掌握催化剂的特点“一变二不变”和催化作用(改变反应速率),了解影响化学反应速率的因素:温度、催化剂、反应物本身的性质,状态等.

练习册系列答案
相关题目
5.某学校化学兴趣小组的同学想测定某同学家装修后剩余大理石中碳酸钙的含量,做了如下实验:首先称取50g该大理石样品,然后将200g的稀盐酸分5次加入(假设其中的杂质既不溶于水也不与盐酸反应)进行充分反应.实验过程中的数据记录如下:
(1)a的数值为30;
(2)写出实验中发生反应的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)根据已知条件列出求解生成二氧化碳总质量(X)的比例式$\frac{100}{44}=\frac{45}{X}$;
(4)第二次反应后所得溶液中溶质质量是24.3%;
(5)某工厂要想制得280t含杂质19%的生石灰,在制备过程中损失了10%的原料,需要这种大理石废料的质量为500t.
| 稀盐酸的质量 | 第一次 40g | 第二次 40g | 第三次 40g | 第四次 40g | 第五次 40g |
| 剩余固体质量 | 40g | ag | 20g | 10g | 5g |
(2)写出实验中发生反应的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)根据已知条件列出求解生成二氧化碳总质量(X)的比例式$\frac{100}{44}=\frac{45}{X}$;
(4)第二次反应后所得溶液中溶质质量是24.3%;
(5)某工厂要想制得280t含杂质19%的生石灰,在制备过程中损失了10%的原料,需要这种大理石废料的质量为500t.
2.下列说法你认为错误的是( )
| A. | 化学变化和化学反应是同一个概念 | |
| B. | 物质发生化学变化时一定同时发生物理变化 | |
| C. | 需要加热才会发生的变化一定是化学变化 | |
| D. | 物质的性质决定了变化,物质的变化反映了物质的性质 |
19.下列氧化反应中,不属于化合反应的是( )
| A. | 磷+氧气→五氧化二磷 | B. | 硫+氧气→二氧化硫 | ||
| C. | 氢气+氧气→水 | D. | 乙醇+氧气→二氧化碳+水 |
20.下列变化属于物理变化的是( )
| A. | 纸张燃烧 | B. | 白磷自燃 | ||
| C. | 分离液态空气制氧气 | D. | 食物腐烂 |

