题目内容
5.某学校化学兴趣小组的同学想测定某同学家装修后剩余大理石中碳酸钙的含量,做了如下实验:首先称取50g该大理石样品,然后将200g的稀盐酸分5次加入(假设其中的杂质既不溶于水也不与盐酸反应)进行充分反应.实验过程中的数据记录如下:| 稀盐酸的质量 | 第一次 40g | 第二次 40g | 第三次 40g | 第四次 40g | 第五次 40g |
| 剩余固体质量 | 40g | ag | 20g | 10g | 5g |
(2)写出实验中发生反应的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)根据已知条件列出求解生成二氧化碳总质量(X)的比例式$\frac{100}{44}=\frac{45}{X}$;
(4)第二次反应后所得溶液中溶质质量是24.3%;
(5)某工厂要想制得280t含杂质19%的生石灰,在制备过程中损失了10%的原料,需要这种大理石废料的质量为500t.
分析 (1)根据第一次加入40g稀盐酸,导致固体由50g变成了40g,减少了10g,第三次也是有20g变成10g,说明每加入40g盐酸能够使固体减少10g,依据杂质不与盐酸反应,反应的是碳酸钙,结合方程式计算出所用稀盐酸溶质的质量分数,并据溶质的质量分数式分析解答;
(2)碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,据此书写方程式;
(3)第5次加入40g盐酸,固体减少5g,说明样品中碳酸钙反应完毕,依据碳酸钙的总质量计算生成的二氧化碳的总质量,列出比例式;
(4)利用第二次实验所消耗碳酸钙的量,根据反应的化学方程式,计算出生成的氯化钙的质量,由溶质的质量分数公式,求出加入水后溶液中溶质的质量分数;
(5)由50g样品中杂质的质量是5g,计算样品中碳酸钙的纯度,并据碳酸钙分解的反应方程式计算需要大理石的质量
解答 解:(1)第一次加入40g稀盐酸,导致固体由50g变成了40g,减少了10g,第三次也是有20g变成10g,说明每加入40g盐酸反应10g碳酸钙,即a=40g-10g=30g;
(2)碳酸钙和盐酸反应方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)要求生成二氧化碳的总质量,则须求出所有碳酸钙反应生成的二氧化碳的质量,第5次加入40g盐酸,固体减少5g,说明样品中碳酸钙反应完毕,所以碳酸钙的总质量是50g-5g=45g
设45g碳酸钙与盐酸反应生成二氧化碳的总质量是X
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
45g X
则求解生成二氧化碳总质量的比例式是:$\frac{100}{44}=\frac{45}{X}$;
(4)第二次反应的碳酸钙的质量是20g,设生成的二氧化碳的质量是a,生成氯化钙的质量是b
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
20g b a
$\frac{100}{20g}=\frac{111}{b}=\frac{44}{a}$
b=22.2g
a=8.8g
所以向第二次反应后所得溶液的溶质质量分数是$\frac{22.2g}{20g+80g-8.8g}$×100%=24.3%;
(5)根据以上分析,该大理石中碳酸钙的质量分数是:$\frac{45g}{50g}$×100%=90%
设需要这种大理石的质量为n
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 56
n×90% 280t×(1-10% )
$\frac{100}{n×90%}=\frac{56}{280t×(1-10%)}$
n=500t
故答案为:
(1)30;
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)$\frac{100}{44}=\frac{45}{X}$;
(4)23.4%;
(5)500t.
点评 本题考查综合、全面,分析透彻每次加入40g稀盐酸固体剩余物质量的变化,对反应进行的情况进行判断,这是解决本题的基础,该题可很好考查学生分析、解决问题的能力,本题涉及的方程式计算较多,要找准已知量,细心分析.

A.在化学反应后其质量减小 B.在化学反应后其化学性质发生了变化
C.能增大生成物的质量 D.能改变化学反应速率
【提出问题】在过氧化氢溶液的分解反应中,除了二氧化锰,是否有其他物质也能作催化剂?
【查阅资料】在过氧化氢溶液的分解反应中,氧化铜也能作催化剂.
【进行实验】用天平称量0.2g氧化铜,取5mL5%过氧化氢溶液于试管中,进行如下实验:
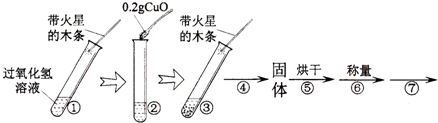
(1)填写表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦操作 | 结论 |
| 剧烈反应,有气泡产生,带火星的木条复燃 | 称量的氧化铜的质量仍为0.2g | 重复步骤溶液中有气泡放出,带火星的木条复燃 | 在过氧化氢溶液的分解反应中,氧化铜也能作催化剂 |
| A. | 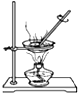 蒸发 | B. | 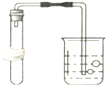 检查装置气密性 | C. | 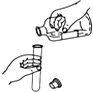 取用液体 | D. | 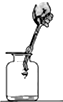 铁丝在O2中燃烧 |
(1)氧气有很多用途.下列属于氧气用途的是A和C(填序号).
A.医疗急救 B.食品防腐 C.航天火箭 D.霓虹灯
(2)氧气能跟很多物质反应.根据如图所示实验,并阅读资料,回答下列问题.

Ⅰ.小明对图1铁丝在氧气中燃烧为什么会火星四射进行探究.下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录.请你分析回答:
| 物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧时 的现象 | 剧烈燃烧,发出 耀眼白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | 未填 |
②铁丝在氧气燃烧的文字表达式是铁+氧气$\stackrel{点燃}{→}$四氧化三铁.集气瓶底部放少量水或细沙的作用是防止生成物溅落瓶底,使集气瓶炸裂;
③通过以上探究,你认为铁丝燃烧产生火星四射现象的原因可能是铁丝中含碳量≥0.6%.
Ⅱ.图2中的反应现象为硫剧烈的燃烧,发出明亮的蓝紫色火焰,反应的文字表达式为硫+氧气$\stackrel{点燃}{→}$二氧化硫,集气瓶中加入的液体可能是氢氧化钠溶液,其主要目的是吸收反应生成的二氧化硫.
| A. |  | B. |  | C. |  | D. |  |
 (1)空气的成分按体积百分数计算,大约是氮气占78%,氧气占21%,稀有气体占0.94%,二氧化碳占0.03%.
(1)空气的成分按体积百分数计算,大约是氮气占78%,氧气占21%,稀有气体占0.94%,二氧化碳占0.03%.