题目内容
1.混合气体由CO、CO2、H2、N2组成,依次通过足量灼热的焦炭、灼热的氧化铜、澄清石灰水,最后得到的气体( )| A. | N2和H2 | B. | N2和CO2 | C. | N2和H2O | D. | N2和CO |
分析 灼热的焦炭能与二氧化碳反应生成一氧化碳,可用于除去混合气体中的二氧化碳;灼热的氧化铜可与混合气体中的氢气、一氧化碳等还原性气体反应,可除去氢气和一氧化碳;澄清石灰水可吸收二氧化碳,用于除去混合气体中的二氧化碳;据此进行分析判断.
解答 解:混合气体由CO、CO2、H2、N2组成,依次通过足量灼热的焦炭,二氧化碳与焦炭反应,二氧化碳被除去;再灼热的氧化铜,氢气、一氧化碳与灼热的氧化铜反应分别生成铜和水、铜和二氧化碳,氢气、一氧化碳吸收,但生成了水和二氧化碳;最后通过澄清石灰水,二氧化碳与石灰水反应生成碳酸钙沉淀和水,故最后得到的气体是N2和H2O.
故选:C.
点评 本题难度不大,熟练掌握常见气体的性质是正确解答此类题的关键;解题时要注意在反应中是否生成了新的气体,从而准确判断最后得到的气体.

练习册系列答案
相关题目
11. 某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀盐酸加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式HCl+NaOH═NaCl+H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
【假设猜想】甲组同学的猜想如下:
猜想一:溶质是NaCl与NaOH 猜想二:溶质只是NaCl 猜想三:溶质是HCl和NaCl.
【实验探究】
(1)乙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH.
(2)为了验证其余猜想,丙组同学想选用碳酸钠溶液完成实验,填写以下表格:
【实验反思】氢氧化钠与稀盐酸发生中和反应观察不到明显现象,为了确定其反应是否反生,丁组同学设计了如下的实验方案:先用pH试纸测定氢氧化钠溶液的pH,然后向其中滴加稀盐酸,边滴边测定混合溶液的pH.请你分析上述方案中,为什么要“当测定pH小于或等于7,”才可证明发生反应了,其原因是排除因稀盐酸的加入,稀释氢氧化钠溶液而引起pH减小的干扰.
【实验拓展】如图是氢氧化钠溶液与盐酸反应的微观示意图.
反应的实质:氢氧化钠与盐酸反应的实质是氢氧根离子(OH-)与氢离子(H+)结合生成水.
 某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).【演示实验】将一定量的稀盐酸加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式HCl+NaOH═NaCl+H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
【假设猜想】甲组同学的猜想如下:
猜想一:溶质是NaCl与NaOH 猜想二:溶质只是NaCl 猜想三:溶质是HCl和NaCl.
【实验探究】
(1)乙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH.
(2)为了验证其余猜想,丙组同学想选用碳酸钠溶液完成实验,填写以下表格:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量反应后的溶液于试管中,逐滴加入碳酸钠溶液. | 有气泡产生 | 猜想三正确 |
【实验拓展】如图是氢氧化钠溶液与盐酸反应的微观示意图.
反应的实质:氢氧化钠与盐酸反应的实质是氢氧根离子(OH-)与氢离子(H+)结合生成水.
9.在反应X+2Y═R+2M中,已知R和M的相对分子质量之比为22:9,当1.6克X与Y完全反应后,生成4.4克R,则在反应中X与Y的相对分子质量之比为( )
| A. | 8:16 | B. | 23:9 | C. | 32:9 | D. | 16:9 |
16.有关碳和碳的氧化物的下列说法中正确的是( )
| A. | C60是由碳原子构成的单质 | |
| B. | 石墨转变成金刚石的变化是化学变化 | |
| C. | 二氧化碳有毒使人窒息而亡 | |
| D. | 焦炭具有可燃性故用于冶金工业 |
11.下列实验现象描述不正确的是( )
| A. | 红磷燃烧产生大量的白烟 | |
| B. | 木炭在空气中燃烧,生成二氧化碳气体 | |
| C. | 硫在空气中燃烧,产生淡蓝色火焰 | |
| D. | 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 |
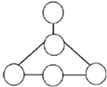 整理、归纳物质性质之间的相互联系,是化学学习的一种有效方法.小丽在复习单质、氧化物、酸、碱、盐性质时,构建了右边知识网络图,图中短线“-”表示相连的两种物质能在一定条件下发生反应.我能帮小丽在单质、氧化物、酸、碱、盐五类物质中分别选取一种物质,将它们的化学式填写在图中圆圈中,并符合以上要求.
整理、归纳物质性质之间的相互联系,是化学学习的一种有效方法.小丽在复习单质、氧化物、酸、碱、盐性质时,构建了右边知识网络图,图中短线“-”表示相连的两种物质能在一定条件下发生反应.我能帮小丽在单质、氧化物、酸、碱、盐五类物质中分别选取一种物质,将它们的化学式填写在图中圆圈中,并符合以上要求.