题目内容
14.下列物质露置在空气中一定不会发生化学变化的是( )| A. | 生石灰 | B. | 氢氧化钠 | C. | 纯铝制品 | D. | 浓硫酸 |
分析 化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
解答 解:A、生石灰和水反应过程中有新物质氢氧化钙生成,属于化学变化.
B、氢氧化钠和二氧化碳反应过程中有新物质碳酸钠等生成,属于化学变化.
C、纯铝制品和氧气反应过程中有新物质氧化铝生成,属于化学变化.
D、浓硫酸吸收水分过程中没有新物质生成,属于物理变化.
故选D.
点评 本题难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.

练习册系列答案
相关题目
4.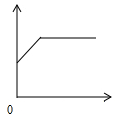 下列各选项与如图所示曲线相符的是( )
下列各选项与如图所示曲线相符的是( )
 下列各选项与如图所示曲线相符的是( )
下列各选项与如图所示曲线相符的是( )| 选项 | 实验操作 | 横坐标 | 纵坐标 |
| A | 向一定质量的锌粉中加入稀硫酸 | 加入稀硫酸的质量/g | 生成氢气的质量/g |
| B | 向一定质量的硝酸银溶液中加入铜粉 | 加入铜粉的质量/g | 溶液的质量/g |
| C | 向一定质量的稀盐酸中不断加入碳酸钙粉末 | 加入碳酸钙的质量/g | 溶液的质量/g |
| D | 向氯化钠饱和溶液中加入水 | 加入水的质量/g | 溶质的质量/g |
| A. | A | B. | B | C. | C | D. | D |
9.经测定,在任何水溶液中,均存在一定数量的H+〔用n(H+)表示〕和一定数量的OH-〔用n(OH-)表示〕,n(H+)与n(OH-)的相对大小对应溶液的酸碱性如表所示:
据此分析:
(1)常温下测得水中pH=7,可知水中n(H+)=n(OH-)(填“>”或“=”或“<”,下同).
(2)向盛有碳酸钠溶液的试管中滴入几滴酚酞,现象是溶液变为红色,原因是该溶液中n(H+)<n(OH-).
| n(H+)与n(OH-)的相对大小 | 溶液的酸碱性 |
| n(H+)>n(OH-) | 酸性 |
| n(H+)=n(OH-) | 中性 |
| n(H+)<n(OH-) | 碱性 |
(1)常温下测得水中pH=7,可知水中n(H+)=n(OH-)(填“>”或“=”或“<”,下同).
(2)向盛有碳酸钠溶液的试管中滴入几滴酚酞,现象是溶液变为红色,原因是该溶液中n(H+)<n(OH-).
19.下列实验操作正确的是( )
| A. |  过滤操作 | B. |  取用药品 | C. |  读出液体体积 | D. |  称量药品 |
6.锡是一种银白色熔点低的金属,是大名鼎鼎的“五金”之一,下列说法中错误的是( )


| A. | 锡原子的核内质子数为50 | |
| B. | 锡的化学性质比较活泼,在化学反应中易得电子 | |
| C. | Sn可以表示一个原子 | |
| D. | 锡的相对原子质量为118.7 |


