题目内容
11.在实验室中,老师用下面所示的装置进行实验(图中固定试管的仪器已略去):加热一段时间后,观察到木炭粉的质量明显减少;氧化铜粉下部出现了一层红亮的铜;澄清石灰水变浑浊.停止加热并冷却到室温.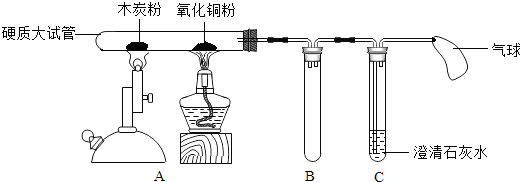
(1)写出硬质大试管中氧化铜发生的化学反应方程式:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 ;
(2)B装置的作用是防止反应后冷却到室温时,C装置的溶液倒流;
(3)实验后要从硬质大试管的剩余固体中回收金属铜.设计实验如下:将可能未完全反应的氧化铜粉剩余物倒入烧杯中,加入过量稀硫酸;当看到黑色固体全部溶解后;加入过量的铁粉并不断用玻璃棒搅拌至反应完全;过滤,洗涤,干燥;用磁铁吸引出过量的铁即可;
(4)该实验证明氧化铜被还原的依据是氧化铜粉下部出现了一层红亮的固体.
分析 (1)利用现象结合硬质试管中物质的性质分析反应的发生.
(2)反应后容器内气体冷却后容器内压强减小,C装置中的溶液会倒流,加入B装置可防止溶液进入硬质大试管中.
(3)利用氧化铜能与酸反应,结合湿法炼铜的原理进行分析并回收到铜即可.
(4)根据实验现象分析解答;
解答 解:(1)在硬质试管中含有碳、氧化铜及氧气,根据现象可知生成了铜所以硬质试管中生成了一氧化碳,石灰水变混浊所以可发生碳与氧气生成二氧化碳,一氧化碳可还原氧化铜、以及碳还原二氧化碳的过程.
故答案为:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 ;
(2)反应后容器内气体冷却后容器内压强减小,C装置中的溶液会倒流,加入B装置可防止溶液倒流入硬质大试管中.
故答案为:防止反应后冷却到室温时,C装置的溶液倒流;
(3)氧化铜能与硫酸反应生成硫酸铜,湿法炼铜的原理是铁与硫酸铜的反应,所以考虑用铁置换出硫酸铜中的铜,过滤后再将剩余的铁粉用磁铁进行去除即可.
故答案为:过量稀硫酸;黑色固体全部溶解;过滤,洗涤,干燥;
(4)该实验证明氧化铜被还原的依据是氧化铜粉下部出现了一层红亮的固体;
故答案为:氧化铜粉下部出现了一层红亮的固体;
点评 此题是一道实验的综合题,解题的关键是对相关物质性质的分析,另外解题时实验的一些关键现象也常常是解题的重要突破口.

练习册系列答案
相关题目
19.从微观粒子的角度解释下列事实,错误的是( )
| A. | 酒香不怕巷子深--分子在不断运动 | |
| B. | 氯化钠溶液具有导电性--溶液中存在自由移动的离子 | |
| C. | 夏天湿衣服晾干得快--温度越高,分子运动速率越快 | |
| D. | 水通电生成氢气和氧气--同种分子化学性质相同 |
16.下列各组物质,只用一种试剂不能鉴别的是( )
| A. | Na2SO4、FeSO4、NaCl溶液 | B. | NaCl、Na2CO3、KCl | ||
| C. | Cu、Fe2O3、Fe3O4固体 | D. | 磷矿粉、硝酸钾、氯化铵 |
3.下列类推正确的是( )
| A. | 原子核是由质子和中子构成的,则所有原子核中都有质子和中子 | |
| B. | H2SO4、HNO3中都含有氧元素,所以酸中一定含有氧元素 | |
| C. | 金属单质都能导电,则能导电的都是金属单质 | |
| D. | 锌、铁和盐酸反应后溶液的质量增加,所以金属与盐酸反应后溶液质量一定增加 |
1.2010年我国西南的旱灾提醒人们应合理使用水资源,下列说法不正确的是( )
| A. | 灾区饮用水源应尽量远离人畜生活区 | |
| B. | 水质浑浊时可加入明矾使杂质沉降除去 | |
| C. | 饮用水(H2O)和消毒剂过氧化氢(H2O2)都由氢元素和氧元素组成 | |
| D. | 我区某地为发展经济大规模围网养殖 |
 请用所学化学知识解释下列原理.
请用所学化学知识解释下列原理. 医疗上常用3%的过氧化氢溶液进行伤口消毒.若浓度过大,会灼伤皮肤及患处.
医疗上常用3%的过氧化氢溶液进行伤口消毒.若浓度过大,会灼伤皮肤及患处.