题目内容
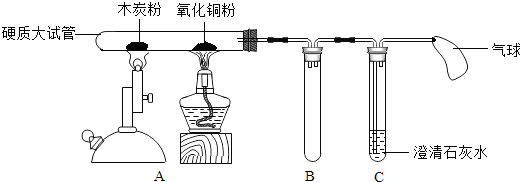
2.对比归纳是学习化学的重要方法.请你根据如图所示回答问题: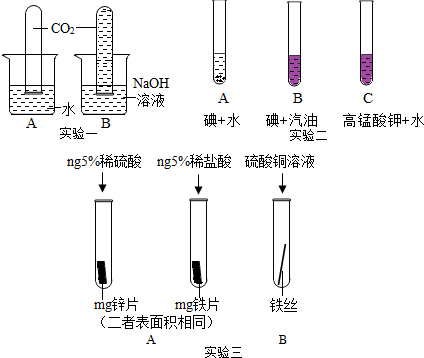
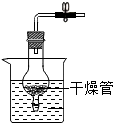
(1)实验一:探究二氧化碳能否与氢氧化钠反应
根据B试管内液面明显高于A试管内液面现象可证明二氧化碳和氢氧化钠发生了化学反应.发生反应的化学方程式是2NaOH+CO2=Na2CO3+H2O.
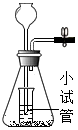
(2)实验二:探究影响物质溶解性的因素.
小王同学做了如图所示的对比实验,发现B中固体可溶,A中几乎不溶.说明影响物质溶解性的因素是溶质的性质;他又补充了C试管的实验,他想探究的影响因素是溶剂的性质.
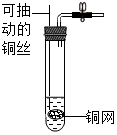
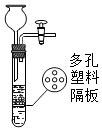
(3)实验三:探究金属活动性
小明以“金属表面产生气泡的快慢”为依据来判断锌、铁的活动性强弱,有同学认为不够合理,理由是选取酸的种类不同.实验B中,若出现铁丝表面有红色的物质现象,可证明铁的活动性强于铜,该反应的化学方程式为Fe+CuSO4═FeSO4+Cu.
分析 (1)根据氢氧化钠与二氧化碳反应生成的碳酸钠能与稀盐酸反应生成了二氧化碳气体分析回答;
(2)对比实验的过程,根据溶解性的大小分析影响溶解性的因素;
(3)根据固定变量法探究物质性质的方法和铁与硫酸铜的反应分析回答.
解答 解:(1)实验一:由于氢氧化钠与二氧化碳反应生成的碳酸钠和水,根据B试管内液面明显高于A试管内液面现象可证明二氧化碳和氢氧化钠发生了化学反应.发生反应的化学方程式是:2NaOH+CO2=Na2CO3+H2O.
(2)实验二:探究影响物质溶解性的因素.
小王同学做了如上图所示的对比实验,发现B中固体可溶,A中几乎不溶.溶质相同,溶剂不同,说明影响物质溶解性的因素是溶剂的性质;他又补充了C试管的实验,在AC中,溶剂相同溶质不同,溶解性不同,他想探究的影响因素是溶质的性质;
(3)实验三:探究金属活动性
小明以“金属表面产生气泡的快慢”为依据来判断锌、铁的活动性强弱.有同学认为不够合理,理由是没控制相同的条件,选取酸的种类不同.实验B中,若出现铁丝的表面有红色物质生成,溶液由蓝色逐渐变为浅绿色 现象,可证明铁的活动性强于铜,该化学反应式为:Fe+CuSO4═FeSO4+Cu.
故答为:(1)B试管内液面明显高于A试管内液面 2NaOH+CO2=Na2CO3+H2O;(2)溶质的性质 溶剂的性质;(3)选取酸的种类不同 铁丝表面有红色的物质 Fe+CuSO4═FeSO4+Cu.
点评 本题利用对比归纳的方法探究了物质的性质,学会利用对比归纳的方法探究物质的物质的性质是化学学习的重要的方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.实验台上摆放着6瓶不同的无色溶液,其中E溶液的试剂瓶标签破损.为此,他们做了如下探究:
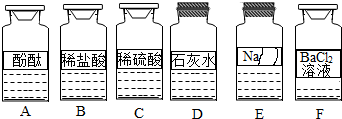
【提出问题】E溶液的成分是什么?
【初步判断】根据受损标签,E溶液不可能是①(填序号)①酸;②碱;③盐.
【提出猜想】猜想Ⅰ:NaOH溶液;猜想Ⅱ:Na2CO3溶液;猜想Ⅲ:Na2SO4溶液.
【设计实验】兴趣小组的同学为验证“猜想Ⅱ”是否正确,设计并完成如下表所示实验.
【分析与推理】
①完成“实验一”后,小鹏即认为“猜想Ⅰ”正确,小明认为“猜想Ⅰ”不一定正确,他的理由是碳酸钠和氢氧化钠溶液均显碱性.
②请写出“实验三”中发生反应的化学方程式Na2CO3+BaCl2=2NaCl+BaCO3↓.
【反思与评价】
①经过讨论,同学们认为“实验一”存在明显操作错误,该错误是把pH试纸浸入待测液;
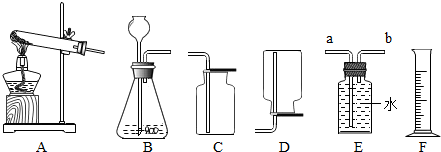
②要在实验室中制备实验二产生的那种气体,发生装置应选择下图中的B,收集装置应选择C,化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.

【提出问题】E溶液的成分是什么?
【初步判断】根据受损标签,E溶液不可能是①(填序号)①酸;②碱;③盐.
【提出猜想】猜想Ⅰ:NaOH溶液;猜想Ⅱ:Na2CO3溶液;猜想Ⅲ:Na2SO4溶液.
【设计实验】兴趣小组的同学为验证“猜想Ⅱ”是否正确,设计并完成如下表所示实验.
| 实验方案 | 实验一 | 实验二 | 实验三 |
| 实验操作 | 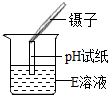 | 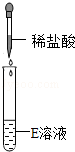 | 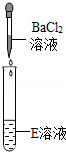 |
| 实验现象 | 试纸变色,对照比色卡,pH>7 | 有无色无味气体产生 | 有白色沉淀产生 |
| 实验结论 | 猜想Ⅱ正确 | ||
①完成“实验一”后,小鹏即认为“猜想Ⅰ”正确,小明认为“猜想Ⅰ”不一定正确,他的理由是碳酸钠和氢氧化钠溶液均显碱性.
②请写出“实验三”中发生反应的化学方程式Na2CO3+BaCl2=2NaCl+BaCO3↓.
【反思与评价】
①经过讨论,同学们认为“实验一”存在明显操作错误,该错误是把pH试纸浸入待测液;
②要在实验室中制备实验二产生的那种气体,发生装置应选择下图中的B,收集装置应选择C,化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.

2.下列化学实验操作中,正确的是( )
| A. | 熄灭酒精灯时,用嘴吹灭 | |
| B. | 滴加药品时,胶头滴管应悬在试管口上方 | |
| C. | 稀释浓硫酸时,把水倒入浓硫酸中 | |
| D. | 将实验时多取的药品放回原试剂瓶中 |
19.“好山、好水、好空气”是贵阳引以为傲的金字招牌,下列气体为空气主要成分之一的是( )
| A. | 氧气 | B. | 一氧化碳 | C. | 二氧化氮 | D. | 二氧化硫 |
12. 实验室制取了两瓶常见的无色气体,放置在实验台上,如图所示.请回答下列问题:
实验室制取了两瓶常见的无色气体,放置在实验台上,如图所示.请回答下列问题:
(1)A气体可能是氢气,A气体的主要用途是做燃料(或冶炼金属等).
(2)请设计实验验证所推断的B气体,完成实验报告.
(3)写出实验室制取B气体的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑等.
 实验室制取了两瓶常见的无色气体,放置在实验台上,如图所示.请回答下列问题:
实验室制取了两瓶常见的无色气体,放置在实验台上,如图所示.请回答下列问题:(1)A气体可能是氢气,A气体的主要用途是做燃料(或冶炼金属等).
(2)请设计实验验证所推断的B气体,完成实验报告.
| 实验步骤 | 实验现象 | 实验结论 |