题目内容
20. 医疗上常用3%的过氧化氢溶液进行伤口消毒.若浓度过大,会灼伤皮肤及患处.
医疗上常用3%的过氧化氢溶液进行伤口消毒.若浓度过大,会灼伤皮肤及患处.(1)现欲将30%的过氧化氢溶液配制成3%过氧化氢溶液1000g用于医用消毒,需要加水900 mL(不用写计算过程).
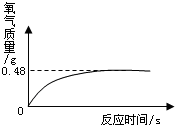
(2)小军欲测定一瓶久置的医用过氧化氢溶液的溶质质量分数,进行了如下实验:取出该溶液50g,加入适量二氧化锰,生成气体质量与反应时间的关系如图所示.计算该溶液中溶质的质量分数.(化学方程式:2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$ 2H2O+O2↑)
分析 溶液稀释前后,溶质质量不变;
过氧化氢在二氧化锰催化作用下分解生成水和氧气,根据氧气质量可以计算过氧化氢质量,进一步可以计算该溶液中溶质的质量分数.
解答 解:(1)设30%的过氧化氢溶液质量为x,
根据题意有:x×30%=1000g×3%,
x=100g,
需要水的质量为:1000g-100g=900g,
需要水的体积为:900g÷1g/mL=900mL,
故填:900.
(2)设过氧化氢质量为y,
由图中可知生成氧气质量是0.48g,
2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$ 2H2O+O2↑,
68 32
x 0.48g
$\frac{68}{x}$=$\frac{32}{0.48g}$,
x=1.02g,
该溶液中溶质的质量分数为:$\frac{1.02g}{50g}$×100%=2.04%,
答:该溶液中溶质的质量分数为2.04%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.“好山、好水、好空气”是贵阳引以为傲的金字招牌,下列气体为空气主要成分之一的是( )
| A. | 氧气 | B. | 一氧化碳 | C. | 二氧化氮 | D. | 二氧化硫 |
5.洗涤是化学实验中的基本操作,下列有关操作合理的是( )
| A. | 使用滴瓶滴加试剂后,立即用蒸馏水洗净滴管并放回原瓶 | |
| B. | 用洗洁精清洗热水瓶里长期积淀的水垢 | |
| C. | 刚加热过高锰酸钾的试管,立即用冷水冲洗 | |
| D. | 过滤时用蒸馏水洗涤滤纸上的硫酸钡沉淀,以除去其表面的可溶性杂质 |
12. 实验室制取了两瓶常见的无色气体,放置在实验台上,如图所示.请回答下列问题:
实验室制取了两瓶常见的无色气体,放置在实验台上,如图所示.请回答下列问题:
(1)A气体可能是氢气,A气体的主要用途是做燃料(或冶炼金属等).
(2)请设计实验验证所推断的B气体,完成实验报告.
(3)写出实验室制取B气体的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑等.
 实验室制取了两瓶常见的无色气体,放置在实验台上,如图所示.请回答下列问题:
实验室制取了两瓶常见的无色气体,放置在实验台上,如图所示.请回答下列问题:(1)A气体可能是氢气,A气体的主要用途是做燃料(或冶炼金属等).
(2)请设计实验验证所推断的B气体,完成实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
9.石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如表:
(1)第三次加入酸反应后,反应是否终止?是(填“是”或“否”).
(2)石灰石样品中碳酸钙的质量分数是.
(3)请计算出四次实验中产生的二氧化碳的总质量(写出计算过程).
| 稀盐酸的用量 | 第一次加入5g | 第二次加入5g | 第三次加入5g | 第四次加入5g |
| 剩余固体质量 | 3g | 2g | 1g | 1g |
(2)石灰石样品中碳酸钙的质量分数是.
(3)请计算出四次实验中产生的二氧化碳的总质量(写出计算过程).
10.规范操作是实验成功的前提,下列实验操作正确的是( )
| A. | 蒸发食盐水时,给蒸发皿加热必须垫上石棉网 | |
| B. | 用排水法收集氧气时,导管口刚有气泡冒出就收集气体 | |
| C. | 用pH试纸测试溶液酸碱性时,应先将pH试纸湿润 | |
| D. | 给试管内的固体药品加热时,试管口应略向下倾斜 |
 已知A、B、C、D、E、F、G、H、I均为初中化学常见的物质.其中E、G为常见的金属,E是目前世界上产量最高的金属,G呈紫红色;I是地壳中含量最高的元素所形成的常见气体单质;人体胃液中含有A,可帮助消化.根据如图所示的转化关系,回答下列问题.(图中反应条件均已略去,反应物和产物均已给出.)
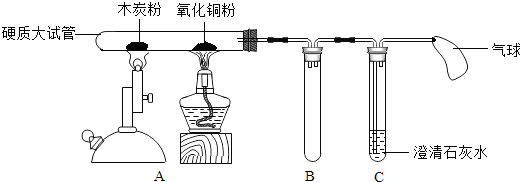
已知A、B、C、D、E、F、G、H、I均为初中化学常见的物质.其中E、G为常见的金属,E是目前世界上产量最高的金属,G呈紫红色;I是地壳中含量最高的元素所形成的常见气体单质;人体胃液中含有A,可帮助消化.根据如图所示的转化关系,回答下列问题.(图中反应条件均已略去,反应物和产物均已给出.) 某化学兴趣小组设计了如图所示实验装置,进行了以下实验.
某化学兴趣小组设计了如图所示实验装置,进行了以下实验.