��Ŀ����
18��̼���γɻ�������������Ԫ�أ���̼��������ѧ��ѧ�о�����Ҫ���ݣ���1������̼��������������������ģ���Ҫ��Ϊ�˼���CO2���ѧʽ�����ŷ�����
��2��ͼ1ΪԪ�����ڱ��е�һ������˵������ȷ����C�����ţ���
A��̼Ԫ�����ڷǽ���Ԫ��
B��̼ԭ�Ӻ���������Ϊ6
C��̼Ԫ�ص�ԭ�ӽṹʾ��ͼΪ
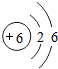
D��̼�����ԭ������Ϊ12.01
��3���ס��ҡ��������dz��л�ѧ�����Ļ���������к���̼Ԫ�أ������������������֮������ͼ2��ʾ��ת����ϵ���������ʺͷ�Ӧ��������ȥ������Ļ�ѧʽΪCaCO3����ת��Ϊ���Ļ�ѧ����ʽΪCaO+H2O=Ca��OH��2��
��4��ͼ3��ijȤζʵ��װ��ͼ����ѹ��ͷ�ιܺɹ۲쵽�����ʹ�������������ԭ��д����ѧ����ʽCO2��ŨNaOH��Һ���գ���ƿ�ڵ���ѹ��С��������ѹ������ƿ�ڵ���ѹ��ʹ�����ʹ�2NaOH+CO2=Na2CO3+H2O��
��5������ͼ4װ�ÿ���CO��ԭFe2O3����ʵ�飬������÷�Ӧ���ɵ���������֪��Aװ����ȡ��CO�����л���������CO2��
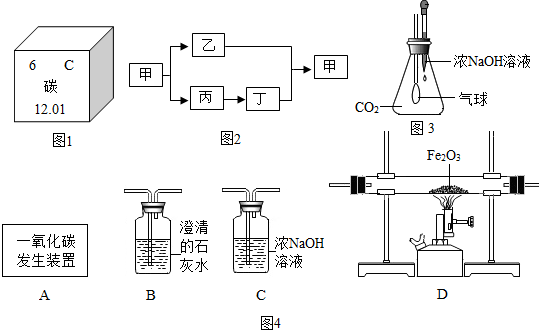
��CO��Fe2O3��Ӧ�Ļ�ѧ����ʽΪFe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
������ͨ��װ�õ�˳����A��C��D��B��װ�ò����ظ�ʹ�ã���
�۴ӻ����Ƕȿ��ǣ�������װ�õĸĽ���ʩ�ǽ�β����ȼ������ռ��ȣ�
��6����ȡ12.5gʯ��ʯ����Ҫ�ɷ���CaCO3�����ʲ��μӷ�Ӧ�������ձ��У������м���50gϡ���ᣬ����ǡ����ȫ��Ӧ����Ӧ����������ձ���ʣ�����ʵ�������Ϊ58.1g���������ձ�����������������ܽ���Բ��ƣ����Լ���ʯ��ʯ��̼��Ƶ�������
���� ����̼��������������������ģ���Ҫ��Ϊ�˼��ٶ�����̼���ŷţ�̼Ԫ�ص�ԭ�ӽṹʾ��ͼ������������Ӧ����4������Ŀ��Ϣ��֪�������к���̼Ԫ�أ����������������˱�����ʯ�ң�����̼��ƣ����Ƕ�����̼��������ʯ�ң�CO��ԭFe2O3��ʵ���У�����Aװ����ȡ��CO�����л���������CO2�����Ҫ��ȥ������̼��Ҫͨ��Cװ�ã�Ȼ����ͨ��Dװ�û�ԭ�������������Bװ�ü����ж�����̼���ɣ���Ϊһ����̼�ж������Ҫ��β������װ�ã���Ӧǰ���ձ��������ļ�������Ϊ���ɵĶ�����̼�����������ݻ�ѧ����ʽ�ж�����̼�����������̼��Ƶ�������
��� �⣺��1������̼��������������������ģ���Ҫ��Ϊ�˼��� ������̼���ŷţ�
��2��̼ԭ�Ӻ��������ӦΪ4�����ӣ���C����
��3�������к���̼Ԫ�أ�������������������ĸ�����������ơ��������ơ�Ũ����ֽ�����Һͱ����ʱ��������ƣ�����̼��ƣ����Ƕ�����̼��������������ˮ�������ɵ��������ƣ�
��4��CO2��ŨNaOH��Һ���գ���ƿ�ڵ���ѹ��С��������ѹ������ƿ�ڵ���ѹ��ʹ�����ʹ� ��ѧ����ʽΪ 2NaOH+CO2=Na2CO3+H2O
��5��CO��Fe2O3��Ӧ�������Ͷ�����̼����ѧ����ʽΪ Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2 ���������̼Ӧ�ó���ʯ��ˮ����˳��ΪC��D��B һ����̼�ж����ŷŵ������л���Ⱦ��������Ӧ��β����ȼ������ռ�������
��6���⣺����CO2������Ϊ��12.5 g+50 g-58.1g=4.4g
��ʯ��ʯ��CaCO3������Ϊx��
CaCO3+2HCl=CaCl2+CO2��+H2O
100 44
x 4.4g
$\frac{100}{x}=\frac{44}{4.4g}$��
x=10g
��ʯ��ʯ�����ʵ�����Ϊ10g��
�ʴ�Ϊ����1��CO2 ��2��C
��3��CaCO3 CaO+H2O=Ca��OH��2
��4��CO2��ŨNaOH��Һ���գ���ƿ�ڵ���ѹ��С��������ѹ������ƿ�ڵ���ѹ��ʹ�����ʹ� 2NaOH+CO2=Na2CO3+H2O
��5����Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2 ��C��D��B
�۽�β����ȼ������ռ��ȣ�
��6��10g��
���� �����ۺϿ�����̼��̼�Ļ���������ʼ����㣬�ۺ���ǿ��Ҫ��ѧ���������ջ���֪ʶ���ܺܺõĽ���⣮

| A�� | 80g | B�� | 40g | C�� | 400g | D�� | 100g |
| A�� | X�Ļ�ѧʽΪCrO3 | |
| B�� | Cr2��SO4��3��CrԪ�صĻ��ϼ�Ϊ+3�� | |
| C�� | �ڷ�Ӧǰ��CrԪ�صĻ��ϼ۽����� | |
| D�� | ��C2H5OH�У�̼Ԫ������Ԫ�ص�������Ϊ1��3 |
| A�� | ʯ����Һ | B�� | ��̪ | C�� | ���� | D�� | ʳ����Һ |
 �����������ӽṹʾ��ͼ������˵������ȷ���ǣ�������
�����������ӽṹʾ��ͼ������˵������ȷ���ǣ�������| A�� | ���DZ�ʾ����ͬһ��Ԫ�� | B�� | ���Ƕ���������ȶ��Ľṹ | ||
| C�� | ���ǵĺ����������ͬ | D�� | �������α�ʾԭ�ӡ����ӡ����� |
| A�� | ԭ����ԭ�Ӻ��ڵ���������������һ����� | |
| B�� | ��ѧ��Ӧǰ��Ԫ�ص�ԭ�Ӹ���һ����� | |
| C�� | ͬ��Ԫ�ص�ԭ�Ӻ����Ӻ��������һ����� | |
| D�� | ��m��ʳ�η���n��ˮ�У��õ���Һ������m��ʳ�κ�n��ˮ��������һ����� |
| A�� |  | B�� |  | C�� |  | D�� |  |