题目内容
13.取一未知质量分数的Na2SO4溶液10克,加入过量的BaCl2溶液,将产生的白色沉淀洗涤干燥后称重,质量为4.66克,求Na2SO4溶液的质量分数.(各元素的相对原子量:O=16,S=32,Ba=137,Na=23,Cl=35.5)分析 根据生成的沉淀的质量和方程式中硫酸钠与硫酸钡的质量比求出硫酸钠的质量质量,再根据溶质的质量分数的计算方法求出样品中硫酸钠的质量分数.
解答 解:设反应的Na2SO4的质量为x
Na2SO4+BaCl2═BaSO4↓+2NaCl.
142 233
x 4.66g
$\frac{142}{x}=\frac{233}{4.66g}$
x=2.84g
硫酸钠溶液溶质的质量分数是:$\frac{2.48g}{10g}$×100%=24.8%
答:Na2SO4溶液的溶质质量粉数:24.8%.
点评 本题考查了学生依据方程式计算的能力,同时考查了溶液中溶质的质量分数,难度不大.

练习册系列答案
相关题目
3. 如图是A、B、C三种物质的溶解度曲线,其中正确的是( )
如图是A、B、C三种物质的溶解度曲线,其中正确的是( )
 如图是A、B、C三种物质的溶解度曲线,其中正确的是( )
如图是A、B、C三种物质的溶解度曲线,其中正确的是( )| A. | t1℃时,等质量的A、B、C三种物质的溶液中溶质质量分数关系为C>A=B | |
| B. | 在t2℃时,A、C两种物质的饱和溶液中,所含溶质质量相等 | |
| C. | 若t1℃时,A物质的溶解度为25g,则在此温度下,该物质的溶液中溶质质量分数最大不会超过20% | |
| D. | t1℃时,将A、B、C三种物质的饱和溶液升温到t3℃,所得溶液中溶质的质量分数由大到小的顺序为A>B=C |
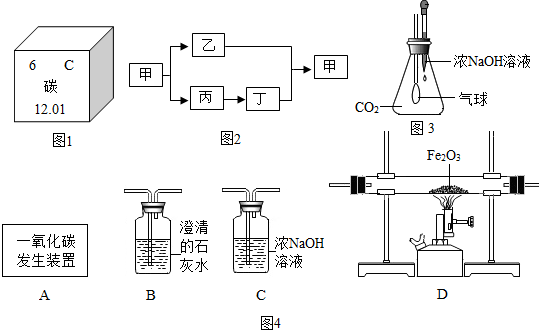
1.如图为某化工企业生产流程示意图:下列说法正确的是( )

| A. | 钛酸亚铁(FeTiO3)中钛元素为+3价 | |
| B. | ①中反应为:2FeTiO3+6C+7Cl2$\frac{\underline{\;一定条件\;}}{\;}$2X+2TiCl4+6CO,则X为FeCl2 | |
| C. | ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为1:2 | |
| D. | ③中氩气(Ar)作保护气,反应类型为置换反应 |
8.下列关于各种材料的说法中正确的是( )
| A. | 陶瓷、橡胶、水银、碳都是很好的绝缘材料 | |
| B. | 金、银、铜等都是很好的导体 | |
| C. | 铝、碳、铁、玻璃都是很好的磁性材料 | |
| D. | 超导体是一种电阻很大的材料 |
2.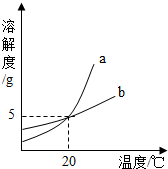 如图是a、b两种固体物质的溶解度曲线,下列说法中正确的是( )
如图是a、b两种固体物质的溶解度曲线,下列说法中正确的是( )
 如图是a、b两种固体物质的溶解度曲线,下列说法中正确的是( )
如图是a、b两种固体物质的溶解度曲线,下列说法中正确的是( )| A. | 20oC时,将100g a的饱和溶液蒸干可以得到5g a物质 | |
| B. | 在20℃时,a、b溶液中溶质的质量分数相同 | |
| C. | Ca(OH)2的溶解度曲线与b相似 | |
| D. | 从a的饱和溶液得到a物质的大量固体可以用冷却的方法 |
3.下列除去混合物中少量杂质(括号内为杂质)的方法中,不合理的是( )
| 混合物 | 思路方法 | 选用物质 |
| A.CO(CO2) | 吸收 | 过量的氢氧化钠溶液 |
| B.CaCl2(HCl) | 转化、过滤 | 过量的碳酸钙 |
| C.HCl(BaCl2) | 沉淀、过滤 | 过量的硫酸铜溶液 |
| D.FeSO4(CuSO4) | 置换、过滤 | 过量的铁粉 |
| A. | A | B. | B | C. | C | D. | D |