题目内容
13.欲除去氯化钙溶液中含有的少量盐酸,在不用指示剂的条件下,应加入的试剂是( )| A. | 生石灰 | B. | 碳酸钙粉末 | C. | 氢氧化钙溶液 | D. | 氢氧化钠溶液 |
分析 本题属于除杂质题,一般的除杂质题必须同时满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应②反应时不能加入新的杂质.对于本题中的杂质少量盐酸,在不用指示剂的条件下,应加入的试剂是碳酸钙粉末,碳酸钙与盐酸反应生成氯化钙和水和二氧化碳,没有气泡冒出时,指明盐酸已经除去.
解答 解:A、生石灰不用指示剂,无法证明盐酸完全反应,故选项错误;
B、杂质少量盐酸,在不用指示剂的条件下,应加入的试剂是碳酸钙粉末,碳酸钙与盐酸反应生成氯化钙和水和二氧化碳,没有气泡冒出时,指明盐酸已经除去;故选项正确;
C、氢氧化钙溶液不用指示剂,无法证明盐酸完全反应,故选项错误;
D、氢氧化钠溶液不用指示剂,无法证明盐酸完全反应,并且氯化钠是新杂质,故选项错误;
故选B
点评 本考点属于物质的除杂或净化的探究,是中考的一个难点,也是学生经常出错的题型.根据物质的溶解性和除杂质的条件,要认真分析,综合把握.还要加强记忆除去常用离子的方法和物质的溶解性,从而突破难点,本考点经常出现在选择题、填空题和实验题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.如表对应的解释错误的是( )
| 序号 | 事实 | 解释 |
| A | 在花园中可闻到花香 | 分子在不断运动 |
| B | 用肉眼不能直接观察到CO2分子 | CO2分子很小 |
| C | 50毫升水与50毫升乙醇混合,混合后总体积小于100毫升 | 分子之间有间隔 |
| D | 冰受热变为水,水受热变为水蒸气 | 分子可以再分 |
| A. | A | B. | B | C. | C | D. | D |
1.属于溶液的是( )
| A. | 矿泉水 | B. | 蒸馏水 | C. | 番茄酱 | D. | 泥沙水 |
1.下列图象所表示的意义正确的是( )
| A. | 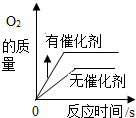 用等质量等浓度过氧化氢溶液来制取氧气 | |
| B. |  用等质量Mg和Fe分别与等质量等浓度的足量稀盐酸反应 | |
| C. |  用等质量石灰石分别与等质量等浓度的足量稀盐酸反应 | |
| D. |  某温度下,向一定量饱和的硝酸钾溶液中不断加入硝酸钾固体 |
5. 学习完“酸、碱、盐的性质”后,老师将两瓶未贴标签的饱和石灰水、饱和碳酸钠溶液分别标记为甲、乙.请你和同学们一起完成探究过程:
学习完“酸、碱、盐的性质”后,老师将两瓶未贴标签的饱和石灰水、饱和碳酸钠溶液分别标记为甲、乙.请你和同学们一起完成探究过程:
【设计实验】
【科学探究】
(1)碳酸钠属于盐(选填“酸”、“碱”、“盐”)类物质,其水溶液显碱性.
(2)现象A是有气泡产生,则甲溶液是碳酸钠;产生该现象的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑;该反应属于基本反应类型中的复分解反应,步骤①乙溶液中溶质一定有氯化钙.
(3)根据步骤③实验现象则上层溶液中一定含有的溶质是氯化钠(酸碱指示剂除外),可能含有的溶质是氯化钙为验证可能含有的溶质,应该补充的实验操作是取样,滴加碳酸钠溶液.
【定量分析】
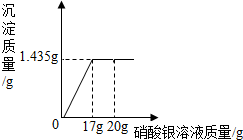
(4)已知酚酞与硝酸银不反应,同学们利用反应废液缸中的上层清液来测定某硝酸银溶液中溶质的质量分数.取上层清液,滴加硝酸银溶液,产生沉淀的质量变化如图所示,该硝酸银溶液溶质的质量分数为10%.
 学习完“酸、碱、盐的性质”后,老师将两瓶未贴标签的饱和石灰水、饱和碳酸钠溶液分别标记为甲、乙.请你和同学们一起完成探究过程:
学习完“酸、碱、盐的性质”后,老师将两瓶未贴标签的饱和石灰水、饱和碳酸钠溶液分别标记为甲、乙.请你和同学们一起完成探究过程:【设计实验】
| 实验操作 | 实验现象 |
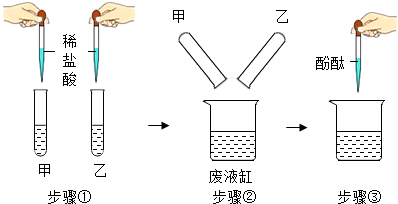 | 步骤①:甲溶液中观察到现象A, 乙溶液中无明显现象 步骤②:底部有白色沉淀 步骤③:上层为无色透明的溶液 |
(1)碳酸钠属于盐(选填“酸”、“碱”、“盐”)类物质,其水溶液显碱性.
(2)现象A是有气泡产生,则甲溶液是碳酸钠;产生该现象的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑;该反应属于基本反应类型中的复分解反应,步骤①乙溶液中溶质一定有氯化钙.
(3)根据步骤③实验现象则上层溶液中一定含有的溶质是氯化钠(酸碱指示剂除外),可能含有的溶质是氯化钙为验证可能含有的溶质,应该补充的实验操作是取样,滴加碳酸钠溶液.
【定量分析】
(4)已知酚酞与硝酸银不反应,同学们利用反应废液缸中的上层清液来测定某硝酸银溶液中溶质的质量分数.取上层清液,滴加硝酸银溶液,产生沉淀的质量变化如图所示,该硝酸银溶液溶质的质量分数为10%.
6.下列说法正确的是( )
| A. | 可燃冰能燃烧是因为其主要成分是甲烷 | |
| B. | 泡沫灭火器可用于扑灭电器引起的失火 | |
| C. | 雨水呈酸性的雨就是酸雨 | |
| D. | C02、CO、N02、S02都是有毒有害气体 |
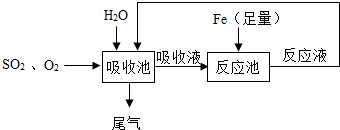 某研究人员按如图所示流程进行“燃煤烟气的脱硫研究”.实验中,SO2和O2混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环.
某研究人员按如图所示流程进行“燃煤烟气的脱硫研究”.实验中,SO2和O2混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环.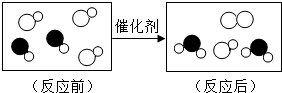 化学与生活、生产密切相关,请用所学的知识下列填空
化学与生活、生产密切相关,请用所学的知识下列填空