题目内容
 小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究.
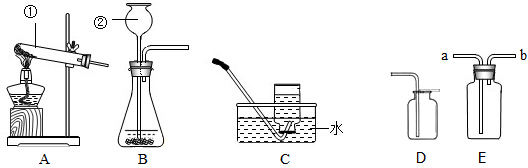
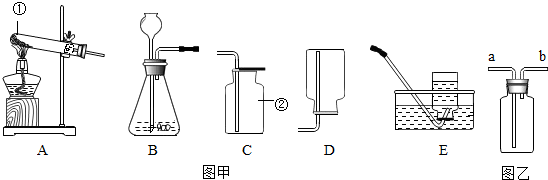
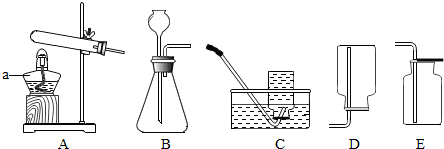
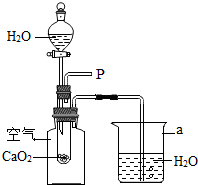
小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究.(1)为研究鱼塘中大量气泡是何种气体所致,小强使用如右图所示的装置进行实验,打开分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃,说明生成的气体是
(2)根据质量守恒定律,小强认为过氧化钙与过量水反应还应产生某种含有钙元素的产物.开始小强假设该产物为CaO,但通过思考他很快否定了原先的假设,并重新假设生成的含钙产物为Ca(OH)2.请解释小强否定原假设建立新假设的理由:
请设计一个实验方案来验证小强的新假设,并填入下表空格中:
| 实验步骤 | 可能出现的现象 | 结论 |
| CaO2与H2O反应有Ca(OH)2生成 |
(4)小强在实验时观察到烧杯中有气泡产生,由此他还得出了什么结论
考点:实验探究物质的性质或变化规律,常用仪器的名称和选用,氧气的检验和验满,碱的化学性质,质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:本题主要围绕过氧化钙与水的反应进行反应生成物的探究,为探究生成物,题中设计了生成物之一氢氧化钙的检验.
(1)氧气的检验,对实验的意义进行评价,常见仪器的识别;
(2)根据质量守恒定律,对反应的生成物进行合理的猜想,结合物质的性质对猜想做出评价;
(3)归纳探究过程,总结反应的化学方程式;
(4)对实验过程中所出现的现象进行分析,归纳出反应的特点.
(1)氧气的检验,对实验的意义进行评价,常见仪器的识别;
(2)根据质量守恒定律,对反应的生成物进行合理的猜想,结合物质的性质对猜想做出评价;
(3)归纳探究过程,总结反应的化学方程式;
(4)对实验过程中所出现的现象进行分析,归纳出反应的特点.
解答:解:(1)能使带火星木条复燃的气体一定是氧气,氧气不易溶于水、可以维持呼吸,为使水中鱼持续获得氧气,需要不断向水中补充氧气.
故答:氧气,补充鱼塘中的氧气,烧杯;
(2)氧化钙极易与水反应生成氢氧化钙,因此,氧化钙不能在水中存在.
故答:在水较多的环境中即使生成CaO,也会和水作用生成Ca(OH)2;
氢氧化钙溶于水溶液呈碱性,滴入酚酞试液会变成红色;向氢氧化钙溶液通入二氧化碳会出现浑浊.
故答:
(3)经过以上的探究,可得知过氧化钙与水反应会放出气体--氧气,同时生成氢氧化钙,
故答:此反应的化学方程式为2CaO2+2H2O=2Ca(OH)2+O2↑;
(4)实验中与广口瓶相连的导管有气泡冒出,是由于广口瓶内气体受热膨胀,热量则来自于过氧化钙与水反应放出的热.故填:CaO2与H2O的反应是放热反应.
故答:氧气,补充鱼塘中的氧气,烧杯;
(2)氧化钙极易与水反应生成氢氧化钙,因此,氧化钙不能在水中存在.
故答:在水较多的环境中即使生成CaO,也会和水作用生成Ca(OH)2;
氢氧化钙溶于水溶液呈碱性,滴入酚酞试液会变成红色;向氢氧化钙溶液通入二氧化碳会出现浑浊.
故答:
| 实验步骤 | 可能出现的现象 | 结论 |
| 取反应后所得的溶液样品滴入酚酞指示剂(或通入CO2 气体) | 变红(或产生白色浑浊) | CaO2与H2O反应有Ca(OH)2生成 |
故答:此反应的化学方程式为2CaO2+2H2O=2Ca(OH)2+O2↑;
(4)实验中与广口瓶相连的导管有气泡冒出,是由于广口瓶内气体受热膨胀,热量则来自于过氧化钙与水反应放出的热.故填:CaO2与H2O的反应是放热反应.
点评:根据质量守恒定律,对反应的生成物进行合理的猜想,结合物质的性质对猜想做出评价.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案
相关题目
T℃时将少量生石灰加到一定质量的饱和澄清石灰水中,溶液的温度升高,再将其恢复到T℃(不考虑水的蒸发),下列四位同学对变化后溶液的分析错误的是( )
| A、溶质的质量分数与原溶液的相同 |
| B、溶剂的质量比原溶液的减少了 |
| C、溶质的质量与原溶液的相同 |
| D、析出固体后的溶液是不饱和溶液 |
下列有关分子、原子和离子的说法正确的是( )
| A、分子是化学变化中的最小的粒子 |
| B、原子是保持化学性质的最小粒子 |
| C、分子、原子、离子都可以直接构成物质 |
| D、在化学反应中,任何离子都不能再分 |