题目内容
5.不属于同素异形体的一组物质是( )| A. | 冰、水 | B. | 氧气、臭氧 | C. | 金刚石、石墨 | D. | 红磷、白磷 |
分析 由同种元素形成的不同种单质互为同素异形体,互为同素异形体的物质要符合以下两个条件:同种元素形成,不同单质;据此进行分析判断.
解答 解:判断同素异形体的关键把握两点:①同种元素形成,②不同单质.
A、冰是固态的水,水是化合物,不是单质,不属于同素异形体,故选项正确.
B、氧气与臭氧(O3)都是由氧元素形成的不同物质,都是单质,互为同素异形体,故选项错误.
C、金刚石和石墨都是由碳元素形成的不同物质,都是单质,互为同素异形体,故选项错误.
D、红磷和白磷都是由磷元素形成的不同物质,都是单质,互为同素异形体,故选项错误.
故选:A.
点评 本题难度不大,判断是否互为同素异形体的关键要把握两点:①同种元素形成,②不同单质,这是解决此类题的关键之所在.

练习册系列答案
相关题目
6.除去下列物质中的少量杂质,所用方法正确的是( )
| 选项 | 物质(括号内为杂质) | 除杂方法 |
| A | NaCl(Na2CO3) | 加入适量的稀盐酸,蒸发、结晶 |
| B | KCl(MnO2) | 加水溶解、过滤、洗涤、干燥 |
| C | CO2(CO) | 通过灼热的氧化铜 |
| D | CaO(CaCO3) | 加入适量的稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
11.某化学兴趣小组为探究复分解反应能否发生,进行了如下实验:
(1)实验②中的现象是有大量气泡产生.
(2)小杨同学认为实验①不反应,小康同学不同意小杨同学的观点,认为无明显现象并不代表没有发生反应.
经小组讨论,设计如下实验来探究稀硫酸与NaOH溶液能否发生反应.

观察到上述实验试管中的现象红色消失(选填“红色消失”或“红色不消失”),说明稀硫酸与NaOH溶液发生了反应,该反应的化学方程式为2NaOH+H2SO4═Na2SO4+2H2O.
(3)反应后,同学们将所有废液倒入同一烧杯中,静置,烧杯中有白色沉淀,溶液呈无色,该无色溶液中一定含有的溶质(除酚酞外)是NaCl(填化学式)
| 实验编号 | ① | ② | ③ |
| 物质 | NaOH溶液 | Na2CO3溶液 | BaCl2溶液 |
| 加稀硫酸后的现象 | 无明显现象 | 有大量气泡产生 | 白色沉淀 |
(2)小杨同学认为实验①不反应,小康同学不同意小杨同学的观点,认为无明显现象并不代表没有发生反应.
经小组讨论,设计如下实验来探究稀硫酸与NaOH溶液能否发生反应.

观察到上述实验试管中的现象红色消失(选填“红色消失”或“红色不消失”),说明稀硫酸与NaOH溶液发生了反应,该反应的化学方程式为2NaOH+H2SO4═Na2SO4+2H2O.
(3)反应后,同学们将所有废液倒入同一烧杯中,静置,烧杯中有白色沉淀,溶液呈无色,该无色溶液中一定含有的溶质(除酚酞外)是NaCl(填化学式)
17.实验是科学探究的重要方法.如图是测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题.

(1)根据下表提供的实验数据,完成下表
(2)装置一和装置二中气球的位置不同,装置二(填“装置一”或“装置二”)更合理,理由是能让空气更易流通,全部通过铜粉,使氧气与铜粉充分反应.
(3)若实验测得的结果偏小(氧气的体积分数小于21%),可能的原因有哪些?(列举两条)铜粉的量不足;
未待装置完全冷却至室温就读数.
(4)若实验测得的结果偏大(氧气的体积分数大于21%),可能的原因有哪些?(列举两条)反应后气球内的气体未挤出便读数;
连接注射器与玻璃管的导管容积过大.

(1)根据下表提供的实验数据,完成下表
| 硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
| 25mL | 15mL | 9mL |
(3)若实验测得的结果偏小(氧气的体积分数小于21%),可能的原因有哪些?(列举两条)铜粉的量不足;
未待装置完全冷却至室温就读数.
(4)若实验测得的结果偏大(氧气的体积分数大于21%),可能的原因有哪些?(列举两条)反应后气球内的气体未挤出便读数;
连接注射器与玻璃管的导管容积过大.
14.锌及其氧化物(ZnO,白色,难溶于水,溶于强酸)具有广泛的应用.
(一)锌的广泛应用
(1)锌被称之为“生命元素”.儿童、青少年如果缺锌严重,将会导致食欲不振和智力发育不良.经常吃贝壳类海产品、红色肉类等含锌的食物有利补“锌”.这里的“锌”是指B.
A.单质 B.元素 C.原子 D.分子
(2)锌与铜熔合可形成“黄铜”,它属于A(选填序号).
A.金属材料 B.无机非金属材料 C.合成材料 D.复合材料
(二)活性ZnO制取的探究
【实验方案】工业上用粗氧化锌(含少量FeO)制取活性氧化锌,其流程如下:
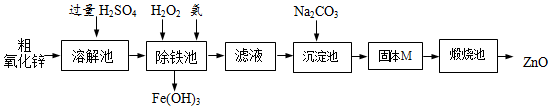
【查阅资料】一些阳离子以氢氧化物形式开始沉淀、完全沉淀时溶液的pH见表.
【问题探究】
(3)“溶解”前将粗氧化锌粉碎成细颗粒,目的是增大接触面积,加快反应速率.
(4)写出在粗ZnO样品中加硫酸发生反应的化学方程式ZnO+H2SO4═ZnSO4+H2O(选写一个).
(5)“溶解”后得到的酸性溶液中含有ZnSO4、H2SO4、FeSO4.除铁池中加入适量H2O2,使Fe2+转化为Fe3+;为使溶液中Fe3+全部转化为Fe(OH)3,而Zn2+不形成Zn(OH)2,则应加入氨水控制溶液的pH的范围为3.2~6.2.
【组成测定】固体B的组成会影响制得的ZnO的活性.为确定aZnCO3•bZn(OH)2•cH2O的组成,进行如下实验(假设每步反应、吸收均完全):
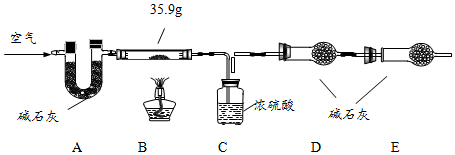
【查阅资料】aZnCO3•bZn(OH)2•cH2O受热分解生成ZnO、H2O、CO2三种产物.
(6)写出装置B中发生反应的化学方程式aZnCO3•bZn(OH)2•cH2O$\frac{\underline{\;\;△\;\;}}{\;}$(a+b)ZnO+aCO2↑+(b+c)H2O .
现称取35.9g aZnCO3•bZn(OH)2•cH2O在B装置中进行完全煅烧,测得装置C和D的质量分别增重7.2g和4.4g.
【实验分析及数据处理】
(7)装置A的作用是除去空气中二氧化碳和水.
(8)根据上述数据,则生成ZnO的质量为24.3 g;a:b:c=1:2:2.
(9)若没有E装置,则测得的a值偏大(填“偏大”、“偏小”或“不变”).
(一)锌的广泛应用
(1)锌被称之为“生命元素”.儿童、青少年如果缺锌严重,将会导致食欲不振和智力发育不良.经常吃贝壳类海产品、红色肉类等含锌的食物有利补“锌”.这里的“锌”是指B.
A.单质 B.元素 C.原子 D.分子
(2)锌与铜熔合可形成“黄铜”,它属于A(选填序号).
A.金属材料 B.无机非金属材料 C.合成材料 D.复合材料
(二)活性ZnO制取的探究
【实验方案】工业上用粗氧化锌(含少量FeO)制取活性氧化锌,其流程如下:

【查阅资料】一些阳离子以氢氧化物形式开始沉淀、完全沉淀时溶液的pH见表.
| 沉淀物 | Fe(OH)3 | Zn(OH)2 | Fe(OH)2 |
| 开始沉淀pH | 1.5 | 6.2 | 6.3 |
| 完全沉淀pH | 3.2 | 8.0 | 9.7 |
(3)“溶解”前将粗氧化锌粉碎成细颗粒,目的是增大接触面积,加快反应速率.
(4)写出在粗ZnO样品中加硫酸发生反应的化学方程式ZnO+H2SO4═ZnSO4+H2O(选写一个).
(5)“溶解”后得到的酸性溶液中含有ZnSO4、H2SO4、FeSO4.除铁池中加入适量H2O2,使Fe2+转化为Fe3+;为使溶液中Fe3+全部转化为Fe(OH)3,而Zn2+不形成Zn(OH)2,则应加入氨水控制溶液的pH的范围为3.2~6.2.
【组成测定】固体B的组成会影响制得的ZnO的活性.为确定aZnCO3•bZn(OH)2•cH2O的组成,进行如下实验(假设每步反应、吸收均完全):

【查阅资料】aZnCO3•bZn(OH)2•cH2O受热分解生成ZnO、H2O、CO2三种产物.
(6)写出装置B中发生反应的化学方程式aZnCO3•bZn(OH)2•cH2O$\frac{\underline{\;\;△\;\;}}{\;}$(a+b)ZnO+aCO2↑+(b+c)H2O .
现称取35.9g aZnCO3•bZn(OH)2•cH2O在B装置中进行完全煅烧,测得装置C和D的质量分别增重7.2g和4.4g.
【实验分析及数据处理】
(7)装置A的作用是除去空气中二氧化碳和水.
(8)根据上述数据,则生成ZnO的质量为24.3 g;a:b:c=1:2:2.
(9)若没有E装置,则测得的a值偏大(填“偏大”、“偏小”或“不变”).
15.下列粒子结构示意图中,表示阳离子的是( )
| A. |  | B. |  | C. |  | D. |  |

 ,则x=38,锶元素的氯化物的化学式为SrCl2.
,则x=38,锶元素的氯化物的化学式为SrCl2.