题目内容
4. 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.(1)甲同学选用如图所示的装置制取氧气.
①写出仪器A的名称:分液漏斗.
②甲同学应选取的试剂是MnO2和H2O2(填化学式),Mn02固体在该反应中起催化作用.
③除用排水法外,甲同学还可选择向上排空气法法收集氧气.
④实验前,甲同学先向仪器A中加入水,然后将导管放人水槽中,并打开仪器A的活塞,观察导管口是否有连续的气泡出现.该实验操作的目的是检验装置气密性.
(2)乙同学称取一定质量KMn04放在大试管中,将温度控制在250℃加热制取O2,该反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.实验结束时,乙同学发现收集到的O2大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】
猜想l:反应生成的MnO2分解放出02;
猜想Ⅱ:反应生成的K2Mn04分解放出O2
做出上述猜想的理由是化学反应前后元素的种类不变.
【实验验证】同学们进行以下实验:
取一定质量的Mn02,在250℃条件下加热一段时间,冷却后测得Mn02的质量不变.则猜想I错误.
分析 (1)①根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
②根据反应装置和所提供药品,确定另一种药品;根据二氧化锰在反应中的催化作用进行分析;
③根据氧气的密度和溶水性考虑收集方法;
④实验前要检验装置的气密性;
(2)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
【提出猜想】有氧气生成就要有氧元素存在;
【实验验证】根据质量的变化分析判断.
解答 解:(1)①通过分析题中所指仪器的作用可知,A是分液漏斗;
②如图装置适合固液不加热反应,我们可以用过氧化氢溶液和固体二氧化锰反应制取氧气,其中二氧化锰在反应前后性质和质量都不发生变化,所以二氧化锰起催化作用;
③因氧气的密度大于空气的密度,不易溶于水,所以除用排水法收集外,还可以用向上排空气法收集;
④这种做法可以使装置内外形成压力差,看装置是否漏气,所以该实验操作的目的是:检验装置的气密性;
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
【提出猜想】O2是由氧元素组成的单质,所以猜想的理由是锰酸钾、二氧化锰中含有氧元素,化学反应前后元素的种类不变;
【实验验证】根据质量守恒定义和冷却后测得Mn02的质量不变可知,猜想I是错误的.
故答案为:(1)①长颈漏斗;
②H2O2,催化;
③向上排空法;
④检测装置的气密性;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,
【提出猜想】化学反应前后元素的种类不变;
【实验验证】I.
点评 本题考查制取氧气的实验以及相关问题,还有验证猜想的实验设计,要同学们具有综合的化学知识才可做好此题.

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案| A. | 加热过氧化氢溶液 | B. | 植物的光合作用 | ||
| C. | 加热氯酸钾和二氧化锰的混合物 | D. | 石蜡燃烧 |
| A. | 硫在空气中燃烧时产生蓝紫色火焰,生成了有刺激性气味的气体 | |
| B. | 红磷在空气中燃烧时生成大量的白雾 | |
| C. | 铁在氧气中燃烧生成四氧化三铁 | |
| D. | 木炭在氧气中燃烧时,发出白光,放出大量的热 |
| A. | 100mL酒精和100mL水混合在一起,体积小于200mL--分子是有质量的 | |
| B. | 湿衣服逐渐变干--分子是运动的 | |
| C. | 气体能被压缩--分子间有间隔 | |
| D. | 水通电分解生成氢气和氧气--分子是可以再分的 |
| A. | 金刚石在液态氧气中燃烧 | B. | 光合作用 | ||
| C. | 干冰升华 | D. | 有机肥的腐熟 |
 某研究性学习小组,选择“过氧化氢(H202)生成氧气(02)的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程.
某研究性学习小组,选择“过氧化氢(H202)生成氧气(02)的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程.【假设】过氧化氢生成氧气的快慢与催化剂的种类有关.
实验方案】常温下,在两瓶相同体积的过氧化氢(H202)溶液中分别加入相同质量的二氧化锰(MnO2)和红砖粉,测量各生成一瓶(相同体积)氧气所需的时间.
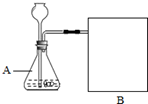
【进行实验】上图是他们进行实验的装置图,气体发生装置中A仪器的名称是锥形瓶,此实验中B处宜采用的气体收集方法是排水法.
【实验记录】
| 实验编号 | 1 | 2 |
| 反应物 | 6%过氧化氢(H202) | 6%过氧化氢(H202) |
| 催化剂 | 1g 二氧化锰 | |
| 时间 | 35s | 152s |
【反思】过氧化氢在常温下分解缓慢,加入二氧化锰或红砖粉后反应明显加快,若要证明二氧化锰(MnO2)和红砖粉是该反应的催化剂,还需增加实验来验证它们在化学反应前后的质量 和化学性质 是否改变.
