题目内容
17.盐酸、硫酸是常见的酸,也是常用的化工原料.在它们的水溶液里由于存在有相同的H+(填离子符号),实验室中浓H2SO4需要密封保存,原因是浓H2SO4具有吸水性.用玻璃棒蘸取少量浓硫酸在滤纸上写字,过后观察,字迹显黑色,这主要是由于浓硫酸具有脱水性.若打开浓盐酸的瓶盖,发现瓶口冒白雾,是因为浓盐酸具有挥发性,因此浓盐酸也要密封保存.分析 理解酸的定义:酸是在水溶液中电离出的阳离子全部是氢离子的化合物,据浓硫酸具有吸水性和脱水性,浓盐酸具有挥发性,进行分析解答.
解答 解:因为酸是在水溶液中电离出的阳离子全部是氢离子的化合物,所以酸在水溶液中具有相同的H+;
实验室中浓H2SO4需要密封保存,原因是浓H2SO4具有吸水性.
用玻璃棒蘸取少量浓硫酸在滤纸上写字,过后观察,字迹显黑色,这主要是由于浓硫酸具有脱水性,将滤纸中的氢、氧元素以水的形式夺走,导致纸张炭化.
若打开浓盐酸的瓶盖,发现瓶口冒白雾,是因为浓盐酸具有挥发性,从浓盐酸中挥发出来的氯化氢气体与空气中的水蒸气结合成盐酸小液滴,因此浓盐酸也要密封保存.
故答案为:H+;吸水;脱水;挥发.
点评 本题难度不大,掌握浓硫酸具有吸水性与脱水性、浓盐酸具有挥发性是正确解答本题的关键.

练习册系列答案
相关题目
7.有限的元素可组成种类繁多的物质,甲、乙、丙、丁、戊五种物质均由下表中的一种或几种元素组成.
(1)甲溶液在黑色固体乙的作用下生成无色气体丙,丙与生命活动息息相关.甲溶液中的溶质是H2O2(用化学式表示).
(2)为了激发学生学习科学的兴趣,老师在课堂上为大家做了一个“燃纸成铁”的趣味实验,将一张滤纸(组成元素为C、H、O)用戊的浓溶液(由上述两种元素组成的黄色液体)湿润,在酒精灯上烘干后点燃,滤纸变黑、红热,最终生成黑褐色物质,老师告诉大家,黑褐色物质中含有单质铁.由此依据质量守恒定律,戊是Fe.(填化学式)
| 元素名称 | 氢 | 氧 | 氯 | 锰 | 铁 |
| 元素符号 | H | O | Cl | Mn | Fe |
(2)为了激发学生学习科学的兴趣,老师在课堂上为大家做了一个“燃纸成铁”的趣味实验,将一张滤纸(组成元素为C、H、O)用戊的浓溶液(由上述两种元素组成的黄色液体)湿润,在酒精灯上烘干后点燃,滤纸变黑、红热,最终生成黑褐色物质,老师告诉大家,黑褐色物质中含有单质铁.由此依据质量守恒定律,戊是Fe.(填化学式)
8.为检测某化工厂排放的废液中是否含有SO42-,同学们设计了如下方案,并进行了实验.
(1)方案Ⅰ和Ⅲ中,结论不成立的方案是Ⅰ,理由是如果溶液中含有银离子时,银离子能和氯离子结合生成不溶于稀盐酸的白色沉淀氯化银.
(2)方案Ⅲ的滤渣中,滴加稀硝酸是为了排除碳酸根离子的干扰.
| 方案 | 步骤 | 现象 | 结论 |
| Ⅰ | ①取样品,滴加BaCl2溶液 ②对步骤①反应后的混合物进行过滤,在滤渣中滴加稀盐酸 | ①有白色沉淀产生 ②无明显现象 | 废液中含有SO42- |
| Ⅱ | ①取样品,滴加过量盐酸 ②在步骤①的溶液中滴加BaCl2溶液 | ①无明显现象 ②有白色沉淀产生 | 废液中含有SO42- |
| Ⅲ | ①取样品,滴加Ba(NO3)2溶液 ②对步骤①产生的混合物进行过滤,在滤渣中滴加稀硝酸 | ①有白色沉淀产生 ②无明显现象 | 废液中含有SO42- |
(2)方案Ⅲ的滤渣中,滴加稀硝酸是为了排除碳酸根离子的干扰.
5. 关于水的电解实验,下列说法正确的是( )
关于水的电解实验,下列说法正确的是( )
 关于水的电解实验,下列说法正确的是( )
关于水的电解实验,下列说法正确的是( )| A. | 这个实验证明了水是由氧气和氢气组成的 | |
| B. | 电解水生成的氢气和氧气质量比为2:1 | |
| C. | 水电解是化学变化 | |
| D. | 实验证明水是一种混合物 |
12.在实验室准备做粗盐提纯的实验时,其中过滤操作需要的仪器是( )
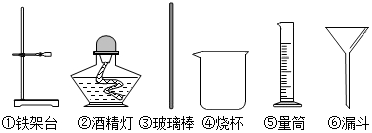

| A. | ①③④⑥ | B. | ①②③⑥ | C. | ②③④⑥ | D. | ①④⑤⑥ |
2.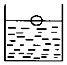 如图在室温下的饱和硝酸钾溶液中放了一个塑料小球.以下做法能使小球下沉的是( )
如图在室温下的饱和硝酸钾溶液中放了一个塑料小球.以下做法能使小球下沉的是( )
 如图在室温下的饱和硝酸钾溶液中放了一个塑料小球.以下做法能使小球下沉的是( )
如图在室温下的饱和硝酸钾溶液中放了一个塑料小球.以下做法能使小球下沉的是( )| A. | 加入少量硝酸钾晶体,充分搅拌 | B. | 蒸发一些溶剂,恢复到室温 | ||
| C. | 升高温度,使硝酸钾晶体析出 | D. | 降低温度,使硝酸钾晶体析出 |
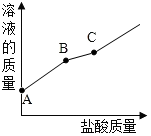 科学就在我们身边,科学知识与我们的生活息息相关.
科学就在我们身边,科学知识与我们的生活息息相关.



