题目内容
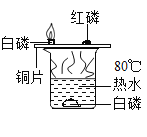
【题目】某同学设计如下实验装置,验证碳的还原性,对实验进行分析并回答:
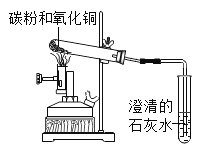
①检查装置气密性的方法是:将导管浸入水中,双手紧握试管,如果_______,说明装置气密性良好。
②当看到澄清的石灰水刚刚出现浑浊时,是否可以确定氧化铜和炭粉已经开始反应? 为什么?_______
③证明碳具有还原性的实验现象是_______,_______;发生反应的化学方程式 依次是_______,_______。
④结束实验的操作是:先_______,再_______。
⑤查阅资料获知,碳与水蒸气在高温下反应,生成两种可燃性气体,这两种气体都能与氧化铜反应,碳与水蒸气反应的化学方程式是_______。
【答案】导管口有气泡产生 不能,试管内的空气中含有氧气,碳与氧气反应也能产生二氧化碳 试管内黑色固体变红 澄清石灰水变浑浊 C+2CuO ![]() 2Cu+CO2↑ Ca(OH)2+CO2=CaCO3↓+H2O 将导气管从试管中撤出 熄灭酒精喷灯 C+H2O
2Cu+CO2↑ Ca(OH)2+CO2=CaCO3↓+H2O 将导气管从试管中撤出 熄灭酒精喷灯 C+H2O![]() H2+CO
H2+CO
【解析】
碳和氧化铜高温生成二氧化碳和铜,二氧化碳和氢氧化钙反应生成碳酸钙和水,碳与水蒸气在高温下反应生成一氧化碳和氢气。
①检查装置气密性的方法是:将导管浸入水中,双手紧握试管,如果导管口有气泡产生,说明装置气密性良好。
②炭粉在氧气中点燃反应生成二氧化碳,看到澄清的石灰水刚刚出现浑浊时,不能确定氧化铜和炭粉已经开始反应,理由是试管内的空气中含有氧气,碳与氧气反应也能产生二氧化碳。
③碳和氧化铜高温生成二氧化碳和铜,二氧化碳能使澄清石灰水变浑浊,二氧化碳和氢氧化钙反应生成碳酸钙和水,故证明碳具有还原性的实验现象是试管内黑色固体变红,澄清石灰水变浑浊;发生反应的化学方程式依次是C+2CuO![]() 2Cu+CO2↑,Ca(OH)2+CO2=CaCO3↓+H2O。
2Cu+CO2↑,Ca(OH)2+CO2=CaCO3↓+H2O。
④为防止澄清石灰水倒吸,结束实验的操作是:先将导气管从试管中撤出,再熄灭酒精喷灯。
⑤碳与水蒸气在高温下反应,生成两种可燃性气体,这两种气体都能与氧化铜反应,碳与水蒸气反应生成的气体是一氧化碳和氢气,反应的化学方程式是C+H2O![]() H2+CO。
H2+CO。

 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案【题目】小滨同学为了测定某珍珠粉中碳酸钙的质量分数,称取12.5g珍珠粉样品,进行四次高温煅烧、冷却、称量剩余固体的重复操作(杂质不参加反应),记录数据如下:
操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量/g | 10.8 | 9.6 | 8.1 | 8.1 |
试计算:
(1)完全反应后生成二氧化碳的质量为____________g;
(2)求该珍珠粉中碳酸钙的质量分数为____________。
【题目】某研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
实验 | 1 | 2 | 3 | 4 |
加入样品的质量/g | 5 | 10 | 15 | 20 |
生成CO2的质量/g | 1.54 | 3.08 | 4.5 | m |
(1)上表中m的数值是_____
(2)试计算这种石灰石矿中碳酸钙的质量分数____。