题目内容
【题目】某研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
实验 | 1 | 2 | 3 | 4 |
加入样品的质量/g | 5 | 10 | 15 | 20 |
生成CO2的质量/g | 1.54 | 3.08 | 4.5 | m |
(1)上表中m的数值是_____
(2)试计算这种石灰石矿中碳酸钙的质量分数____。
【答案】4.5 70%
【解析】
(1)上表可知每5g样品生成1.54g二氧化碳,如果15g样品完全反应,应该生成4.62g二氧化碳,也就是说,15g样品有剩余,m的数值是4.5;
(2)设10克样品中含CaCO3的质量为x,计算过程如下:
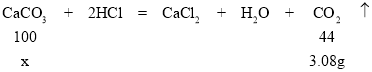
![]() ,解得x=7g,故10g样品中含有碳酸钙的质量为7g,碳酸钙的质量分数为
,解得x=7g,故10g样品中含有碳酸钙的质量为7g,碳酸钙的质量分数为![]() 。
。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目