题目内容
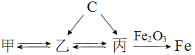
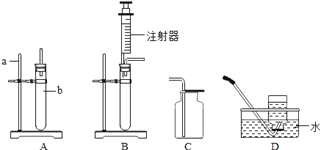
【题目】甲、乙、丙三种固体的溶解度曲线如图1所示,并进行如图2的实验。下列说法正确的是( )

A. 三种物质的溶解度:乙>丙>甲
B. t2℃时,溶质的质量分数:甲=乙
C. t3℃,乙、丙的饱和溶液降温均有溶质析出
D. 图2中试管内所盛饱和溶液的溶质为对应图1溶解度曲线中的丙
【答案】D
【解析】
A、由甲、乙、丙三种固体的溶解度曲线可知,t1℃时,三种物质的溶解度:乙>丙>甲,A选项不正确,不符合题意;
B、由甲、乙、丙三种固体的溶解度曲线可知,t2℃时,甲的溶解度等于乙的溶解度,则t2℃时,甲和乙的饱和溶液溶质的质量分数相等,B选项不正确,不符合题意;
C、由甲、乙、丙三种固体的溶解度曲线可知,乙的溶解度随温度的升高而增大,t3℃,乙的饱和溶液降温有溶质析出;丙的溶解度随温度的升高而减小,t3℃,丙的饱和溶液降温没有溶质析出,C选项不正确,不符合题意;
D、图2中烧杯中加入生石灰,生石灰溶解在水中放出热量,烧杯中溶液温度升高,试管内所盛物质的饱和溶液在温度升高的情况下析出晶体,说明该物质的溶解度随温度的升高而减小,则该溶质为对应图1溶解度曲线中的丙,D选项正确,符合题意。故选D。

【题目】实验是科学探究的重要方法。
实验探究一:气体实验室制法
查阅资料:① 实验室用铜与浓硝酸反应制取NO2气体。
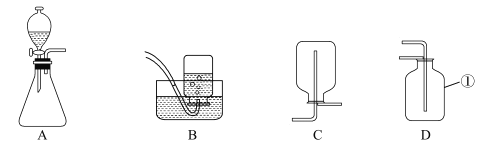
② NO2 是一种红棕色的气体,密度比空气大,能与水反应生成HNO3和NO气体,NO是一种无色气体,NO和NO2都是大气污染物。 根据图所示装置回答有关问题。
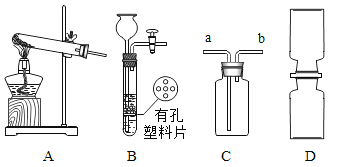
(1)实验室制取NO2气体的发生装置是_____(填装置序号),用C装置收集NO2气体时,NO2应从导管_____(填“a”或“b”)进入。
(2)NO2气体不能用排水法收集的原因(用化学方程式解释)_____。
(3)用D装置演示分子运动实验,为了缩短演示时间,应将盛有NO2的集气瓶 最好放在_____(填“上”或“下”)面,另一瓶是空气。
实验探究二:探究影响化学反应速率的因素 以过氧化氢分解为研究对象进行实验。化学小组均采用如图装置进行实验,记录收集10ml氧气的时间。

实验室提供的试剂:2.5%、5%、10%三种 浓度的H2O2溶液;MnO2;CuO;红砖粉末。 数据记录如下:
实验序号 | H2O2 溶液 | 其他物质质量 | 收集 10ml氧气的时间/s |
① | 5ml10% | 0.5g MnO2 | 10 |
② | 5ml10% | 0.5g 红砖粉末 | 60 |
③ | 5ml10% | 0.5g CuO | 20 |
④ | 5ml5% | 0.5g MnO2 | 15 |
(1)小明通过分析实验①②③的数据。
得出结论:MnO2、CuO对H2O2分解有催化作用,红砖粉末无催化作用。
小洪同学对该结论提出疑问,并补充对比实验,其实验操作为:____。 结果:长时间(大于 100s)后,收集到很少量气体。 结论:红砖粉末_____(选填“有”、“无”)催化作用,三者中_____催化效率最高。 写出实验③的反应化学方程式:_________。
(2)小王同学通过分析实验_____(填实验序号)。 得出结论为:当__________时,反应物浓度越大,反应速率越快。
(3)影响化学反应速率的因素还有____________________________。
实验探究三:二氧化碳气体与氢氧化钠溶液的反应情况。
化学小组用小烧杯盛装一定量的氢氧化钠溶液并通入一定量的CO2气体进行探究。
(提出问题)
氢氧化钠溶液中通入/span>CO2一段时间后所得的溶液(下面称样品)中会有什么溶质?
(查阅资料)
① 通入少量的二氧化碳时,NaOH与CO2反应的化学方程式_____。
② 通入过量的二氧化碳时,反应的化学方程式为Na2CO3+CO2+H2O= 2NaHCO3
③ 碳酸氢盐都能溶于水,BaCO3难溶于水且是白色固体。
④ Na2CO3、NaHCO3的溶液呈碱性、BaCl2 呈中性
(提出猜想)A.溶质是NaOH、Na2CO3; B.溶质是Na2CO3;C.溶质是Na2CO3、NaHCO3; D.溶质是NaHCO3
(设计实验方案)
实验步骤 | 实验现象 | 实验结论 |
取少量样品于试管中, 滴加几滴_______试液(填酸碱指示剂) | 溶液变红色 | 该溶液显碱性 |
②另取少量样品于试管中, 滴加过量的 BaCl2溶液 | 有白色沉淀生成 | 猜想_____不成立 |
③取步骤②静置后的上层清液,滴入稀盐酸 | 有气泡冒出 | 猜想A和B不成立 |
(得出结论)猜想_____成立
(讨论交流)
(1)同学们讨论后一致认为实验步骤①是多余的。 理由是:_____。
(2)若长时间向澄清石灰水中通入二氧化碳会看到什么样的现象呢? 现象是:_____。