题目内容
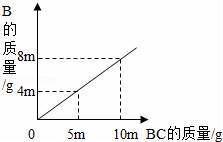
在化学反应A2+BC=B+A2C中,反应物BC与生成物 B的质量关系如图所示.将2g A2与80g BC恰好完全反应,则生成A2C的质量是( )

A.64 g B.18 g C.80 g D.9 g
【考点】质量守恒定律及其应用.
【专题】化学用语和质量守恒定律.
【分析】观察分析图象,由图象可以求出BC与B的质量比,由BC的质量,求出B的质量,再根据质量守恒定律可求出生成A2C的质量.
【解答】解:由图象可知,该反应中BC与B的质量比为10:8;所以,80gBC完全反应生成B的质量是:8×80g÷10=64g.根据质量守恒定律,生成A2C的质量是2g+80g﹣64g=18g.由此可知:
A、生成A2C的质量不是64 g,故A错误;
B、生成A2C的质量是18 g,故B正确;
C、生成A2C的质量不是80 g,故C错误;
D、生成A2C的质量不是9g,故D错误.
故选B.
【点评】本题解题的关键是由图象找出BC与B的质量比,就可以根据质量守恒定律运用化学方程式和物质之间的质量比进行计算.

 名校课堂系列答案
名校课堂系列答案



