��Ŀ����
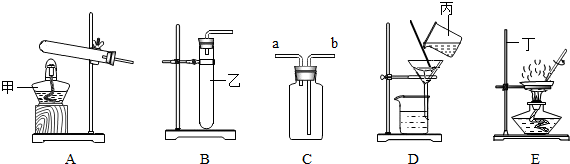
17�� ijͬѧ����ͼ��ʾװ����ȡ�����������CO�����������ʵ�飮���ϣ�
ijͬѧ����ͼ��ʾװ����ȡ�����������CO�����������ʵ�飮���ϣ������£����ᣨHCOOH������ɫ�ӷ���Һ�壬��Ũ�����������ֽ⣮
����ֽ�Ļ�ѧ����ʽΪHCOOH$��_{��}^{Ũ����}$CO��+H2O��
��ʵ��һ���ⶨij�����������Ļ�����������ʵĺ�����
��1��װ��B�е��Լ�������������Һ���������dz�ȥ�ӷ������ļ��װ��C�е��Լ���Ũ���ᣬ����������ˮ����ȼF�оƾ��Ƶ�Ŀ����β����������ֹ��Ⱦ������
��2��E�г���ʯ��ˮ����ǣ���Ӧ�Ļ�ѧ����ʽ��CO2+Ca��OH��2=CaCO3��+H2O��
��3��װ��D�й۲쵽�������Ǻ�ɫ������ڣ���Ӧ�Ļ�ѧ����ʽ��3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
��4��ʵ�����ʱ��Ϩ��ƾ��Ƶ�˳����DAF�����Ӧװ����ţ���
��5������ȡ�û����5.0g����ַ�Ӧ��������ʣ����������Ϊ4.7g��ԭ������������ʵ���������Ϊ80%��
��ʵ������ⶨ��Ʒ�����
��������Ʒ�������������������������������е�һ�ֻ�����ɣ�����ַ�Ӧ��ʵ�����ݼ�¼���£�
| ��Ʒ���� | װ��D�в����ܺ���������� | װ��E������ |
| 2.32g | ��Ӧǰ55.72g | ��Ӧǰ281.00g |
| ��Ӧ��55.08g | ��Ӧ��281.56g |
�ڸ���Ʒ���п��ܵ������Fe3O4��Fe2O3��FeO��Fe3O4��Fe2O3��FeO��
���� ��ʵ��һ���������е�֪ʶ���з�����������̼�����������Ʒ�Ӧ����̼��Ƴ�����ʹ��Һ����ǣ�һ����̼���ж������壬�ŷŵ������л���Ⱦ��������������һ����̼�Ŀ�ȼ�Խ���ȼ�մ�����һ����̼��ԭ�������������Ͷ�����̼���ᵼ�¹����������С����С��������������������Ԫ�ص��������ݴ˿��Խ��н��
��ʵ��������ݱ����ṩ�����ݼ��㣬��ϻ�ѧ����ʽΪ���м��㣮
��� �⣺��1����ȡ�����������CO����Ҫ���ӷ����ļ����һ����̼�л��е�ˮ����������Ҫ��ȥˮ������������Ũ�������ˮ�ԣ�һ����̼���ж������壬�ŷŵ������л���Ⱦ��������������һ����̼�Ŀ�ȼ�Խ���ȼ�մ�����
��2���������ƺͶ�����̼��Ӧ����̼��Ƴ�����ˮ����ѧ����ʽΪ��CO2+Ca��OH��2=CaCO3��+H2O��
��3��һ����̼���������ڸ��µ������·�Ӧ�������Ͷ�����̼��ʵ������Ϊ����ɫ������ڣ���ѧ����ʽΪ��3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
��4��ʵ�����ʱ��Ҫ��ֹͣ��ʢ�й�����Ʒ�IJ����ܼ��ȣ�����ͨ��һ����̼֪����������ȴ������Ҫ��ֹͣD��Ȼ��ֹͣA������һ����̼���ж������壬��F���ֹͣ�����DAF��
��5�����������֪����������������0.3g����������������Ϊx��
3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2 ��m
160 48
x 0.3g
$\frac{160}{x}$=$\frac{48}{0.3g}$
x=1g
����ԭ���������������Ϊ��5g-1g=4g
�����ʵ���������Ϊ��$\frac{4g}{5g}$��100%=80%��
ʵ������ٲ�ѡ��װ��B�������������ǣ�װ��B���ܽ���Ӧ������CO2ȫ�����գ�
�ڸ��ݱ������ݣ�Ҫ�ò��������⣺װ��A���������ԭ������������Ʒ�������������������������Ʒ����Ԫ�ص�����=55.72g-55.08g=0.64g�����������Ԫ�ص���������Ϊ��$\frac{0.64g}{2.32g}$��100%=27.6%����Fe3O4�к�����27.6%����Fe2O3�к�����30%����FeO�к�����22.2%�����Ը���Ʒ���п��ܵ�����ǣ�Fe3O4�� Fe2O3��FeO�� Fe3O4��Fe2O3��FeO��
�ʴ�Ϊ��ʵ��һ����1������������Һ����ȥ�ӷ������ļ��ᣬŨ���ᣬ��ˮ��β����������ֹ��Ⱦ������
��2��CO2+Ca��OH��2=CaCO3��+H2O��
��3��3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
��4��DAF��
��5��80%��
ʵ�������װ��B���ܽ���Ӧ������CO2ȫ�����գ�
��Fe3O4�� Fe2O3��FeO�� Fe3O4��Fe2O3��FeO��
���� �����㿼��������ұ�����ǽ�Ͽα�֪ʶ����Ϣ��������ԭ�����û�ԭ��һ����̼�����������������л�ԭ��������Ϊһ����̼�ж������Ҫ����β�����������������ʵ�����ݵĴ���������ʵ����������ۣ����п�������ص�֮һ��������һ�������ʵ�����У�

��ʵ��1����֤���������ǹ�������ֽⷴӦ�Ĵ���
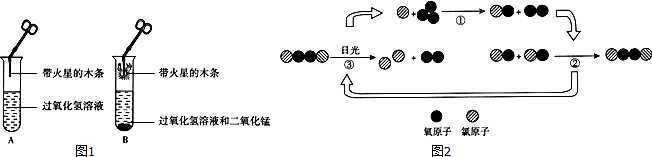
ijͬѧ�������ʵ�飺�ֱ�ȡ5mL5%�Ĺ���������Һ����֧�Թ��У���B���Թ��ڼ��������������̣���ͼ1��ʾ����A�д����ǵ�ľ������ȼ��B�д����ǵ�ľ����ȼ��
A��ľ������ȼ��ԭ����������Ũ�Ȳ�����û������������B�з�Ӧ�Ļ�ѧ����ʽ��2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2����
��ͬѧ��Ϊ����ʵ�鷽��������֤�����������Ǹ÷�Ӧ�Ĵ����������Dz���֤�����������ڷ�Ӧǰ��������ͻ�ѧ����û�иı䣮
��ʵ��2��Ϊ̽���������̶�����طֽ�Ĵ����ã�����ͬ�����£�ͬѧ�ǰ��±�����ʵ�飬����¼������ݣ�������Ӱ��ʵ������ؾ���ͬ��
| ��� | KC103 ����/g | ������������/g | �������� |
| ʵ��1 | 2.0 | / | |
| ʵ��2 | a | Mn02 0.5 |
�ڱ��еĴ�������ָD������ĸ��ţ���
A������������ B����Ӧ����������
C����������� D����λʱ���ڲ������������
����ơ�ʵ��1����Ŀ���ǶԱȣ�
����չ��
��1��ͬѧ�Ǽ���̽�����������Ƿ����������صķֽⷴӦ��
����غͶ������̻�ϼ��ȵĻ�ѧ����ʽΪ��2KClO3$\frac{\underline{MnO_2}}{��}$2KC1+302������֪�������������̻�ϼ���ʱ�����������·�Ӧ���Է�����Ҫ����գ�
��I��2KC103+2Mn02$\frac{\underline{\;\;��\;\;}}{\;}$2KMn04+Cl2��+02����
����2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$K2MnO4+MnO2+O2�����û�ѧ����ʽ��ʾ����
����K2Mn04+Cl2$\frac{\underline{\;\;��\;\;}}{\;}$2KCl+Mn02+02����
ͨ�����Ϸ�����ͬѧ�ǵó����ۣ��������̲���������صķֽⷴӦ��
��2���������ͷų�����ԭ�Ӳ����˳�������ƻ���������ʾ��ͼ��ͼ2���ۺ�ͼ�Т٢ڢ۵ķ�Ӧ���̣�д�������㱻�ƻ��Ļ�ѧ����ʽ��2O3$\frac{\underline{\;\;\;CL\;\;\;}}{�չ�}$3O2��