题目内容
12.某兴趣小组在整理实验室时发现一包氢氧化钙固体,他们根据学过的碱的性质,知道氢氧化钙与空气中的二氧化碳会发生反应生成碳酸钙,于是他们对这包氢氧化钙固体的成分展开探究.【提出问题】这包氢氧化钙固体是否变质?成分是什么?
【猜想假设】猜想一:没有变质,全部是Ca(OH)2;
猜想二:完全变质,全部是碳酸钙.
猜想三:部分变质,既有Ca(OH)2又有CaCO3.
【实验探究】为了探究固体成分,他们分别进行了如下实验:
(1)甲同学取少量固体于试管中,加足量水溶解后滴加酚酞,溶液变红,说明这包固体中含有氢氧化钙.
(2)乙同学取少量固体于试管中,滴加足量稀盐酸,有气泡产生,于是他认为猜想二正确.丙同学认为他的结论不严密,理由是不能排除有氢氧化钙.
(3)为了进一步确定这包固体的成分,丙同学和丁同学设计了以下方案,请你完成下列实验报告:
| 实验步骤 | 可能观察到的现象 | 结论 |
| 丙、取样于烧杯中加水溶解,过滤取少量滤液于试管中通入二氧化碳气体 | 产生白色沉淀 | 有氢氧化钙 |
| 丁、取少量样品于烧杯中,加入适量水溶解,滴加酚酞溶液 后再加入适量稀盐酸 | 先变红,后红色褪去有气泡产生 | 猜想三正确 |
(1)该小组同学反思了氢氧化钙变质的原因,认识到氢氧化钠露置于空气也会变质,请你写出氢氧化钠溶液变质的化学方程式2NaOH+CO2═Na2CO3+H2O.
(2)要除去久置的氢氧化钠固体中的杂质,得到纯净的氢氧化钠固体,可将固体加足量水溶解,加入适量的氢氧化钙(或氢氧化钡)溶液后,产生沉淀后再过滤、蒸发结晶即可.
分析 【猜想假设】该瓶氢氧化钙在保存期间可能吸收空气二氧化碳而全部变质为碳酸钙,也可能部分吸收二氧化碳而部分变质为碳酸钙,也可能因保存较为完善而未变质,可以据此解答该题;
【实验探究】(1)利用变须后的碳酸钙能不溶于水,取样品溶解,向清液中滴加酚酞,观察是否变红检验固体中是否含有氢氧化钙;
(2)取样品溶解,向其中滴加稀盐酸,观察是否有气体放出检验固体是否含有碳酸钙;通过检验固体样品的组成成分可对变质情况进行分析;
(3)考虑二氧化碳与氢氧化钙反应生成白色沉淀,向清液中滴加酚酞,观察是否变红检验固体中是否含有氢氧化钙,可以据此解答该题;
【拓展迁移】
(1)氢氧化钠与空气中的二氧化碳反应生成碳酸钠和水,而使氢氧化钠变质.
(2)在除杂时,所选择的药品只能跟杂质反应,不能跟主物质反应.同时也不能引进新的杂质.利用碳酸钠能与氢氧化钙反应生成氢氧化钠和碳酸钙沉淀,过滤除去沉淀后蒸发即可得纯净氢氧化钠固体.
解答 解:【猜想假设】该瓶氢氧化钙还存在另外两种情况:其一部分氢氧化钙吸收二氧化碳而变质成碳酸;再者也可能保存较好,没有吸收二氧化碳而没发生变质;故猜想二:完全变质,全部是碳酸钙.
【实验探究】
(1)甲同学取少量固体于试管中,加足量水溶解后滴加酚酞,溶液变红,说明这包固体中含有氢氧化钙.
(2)乙同学取少量固体于试管中,滴加足量稀盐酸,有气泡产生,有气体放出检验固体是否含有碳酸钙;但猜想二正确的结论不严密,理由是不能排除有氢氧化钙.
(3)考虑二氧化碳与氢氧化钙反应生成白色沉淀,向清液中滴加酚酞,观察是否变红检验固体中是否含有氢氧化钙:
| 实验步骤 | 可能观察到的现象 | 结论 |
| 丙、取样于烧杯中加水溶解,过滤取少量滤液于试管中通入 二氧化碳气体 | 产生白色沉淀 | 有氢氧化钙 |
| 丁、取少量样品于烧杯中,加入适量水溶解,滴加酚酞溶液 后再加入适量稀盐酸 | 先变红,后红色褪去有气泡产生 | 猜想三正确 |
(1)氢氧化钠与空气中的二氧化碳反应生成碳酸钠和水,而使氢氧化钠变质,故反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O
(2)要除去久置的氢氧化钠固体中的杂质,得到纯净的氢氧化钠固体,可将固体加足量水溶解,加入适量的氢氧化钙(或氢氧化钡)溶液后,产生沉淀后再过滤、蒸发结晶即可.
故答案为:
碳酸钙;(1)氢氧化钙;(2 )不能排除有氢氧化钙;
(3)二氧化碳、先变红,后红色退去有气泡产生;2NaOH+CO2═Na2CO3+H2O;氢氧化钙(或氢氧化钡); 过滤
点评 利用氢氧化钙与碳酸钙性质的不同,设计实验鉴别两物质是否存在,从而判断氢氧化钙变质情况是解本题的关键,另外要熟练写出基本的化学方程式.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
17.4.6g某有机物完全燃烧时需消耗9.6g氧气,生成8.8g二氧化碳和5.4g H2O,该有机物中( )
| A. | 只含碳、氢两种元素 | B. | 只含碳元素 | ||
| C. | 含有碳、氢、氧三种元素 | D. | 可能含氧 |
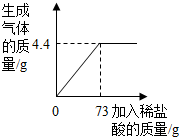 某品牌纯碱中含有杂质NaCl,化学兴趣小组的同学进行了如下实验探究:称取16g样品放入烧杯中,加入稀盐酸至不再产生气泡为止,并绘制出加入稀盐酸的质量与放出气体质量的关系如图:
某品牌纯碱中含有杂质NaCl,化学兴趣小组的同学进行了如下实验探究:称取16g样品放入烧杯中,加入稀盐酸至不再产生气泡为止,并绘制出加入稀盐酸的质量与放出气体质量的关系如图: