题目内容
10.填写化学符号或化学符号表示的意义| 化学符号 | 2Cl |  | 4CO32- | ||||
| 表示意义 | 三 个氮分子 | 核 内 有11个质子 | 五 个银离子 | 硫酸亚铁的化学式 | 氖气的化学式 |
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:元素符号前面加上数字表示几个这样的原子,故2Cl表示2个氯原子;
分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,所以3个氮分子可表示为:3N2;
根据原子结构示意图的意义可知, 核内有11个质子;
核内有11个质子;
离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故五个银离子可表示为:5Ag+;
离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故4CO32-表示为:4个碳酸根离子;
硫酸亚铁是由显+2价的铁元素和显-2价的硫酸根组成,其化学式为:FeSO4;
氖是稀有气体元素,由稀有气体元素组成的单质是单原子分子,所以氖气的化学式就是表示氖元素的元素符号,即:Ne.
故答案为:2个氯原子;3N2;11;5Ag+;4个碳酸根离子;FeSO4;Ne
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

练习册系列答案
相关题目
1.空气成分中,约占总体积的21%是( )
| A. | N2 | B. | H2O | C. | O2 | D. | CO2 |
18.根据表中氯化钠和硝酸钾部分溶解度数据分析、回答下列问题.
(1)10℃时,氯化钠的溶解度是35.8g.
(2)硝酸钾的溶解度随温度的升高而增大;与硝酸钾相比较,氯化钠的溶解度受温度变化影响较小(填“较大”或“较小”).
(3)硝酸钾和氯化钠溶解度曲线的交点在A(填字母序号)之间.
A.20℃~30℃B.30℃~40℃C.40℃~50℃
(4)0℃时,在100g水中加入40g硝酸钾,充分搅拌后,将溶液温度升高到30℃(不考虑水分蒸发),所得溶液是不饱和溶液(填“饱和溶液”或“不饱和溶液”),此时该硝酸钾溶液的溶质质量分数是28.6%(保留一位小数).
(5)实验室中,盐酸和氢氧化钠的中和反应后的溶液中含有氯化钠.某同学将10.0g稀盐酸滴加到溶质质量分数是10.0%的氢氧化钠溶液8.0g中(含2滴酚酞试液),混合液刚好由红色变为无色时可认为恰好完全反应,求:
①所用盐酸中溶质的质量.(计算结果精确到0.01g)
②保持温度为20℃,将反应后的氯化钠的不饱和溶液变成饱和溶液,根据计算写出一种可行的方法.(计算结果精确到0.1g)
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解 度/g | NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
(2)硝酸钾的溶解度随温度的升高而增大;与硝酸钾相比较,氯化钠的溶解度受温度变化影响较小(填“较大”或“较小”).
(3)硝酸钾和氯化钠溶解度曲线的交点在A(填字母序号)之间.
A.20℃~30℃B.30℃~40℃C.40℃~50℃
(4)0℃时,在100g水中加入40g硝酸钾,充分搅拌后,将溶液温度升高到30℃(不考虑水分蒸发),所得溶液是不饱和溶液(填“饱和溶液”或“不饱和溶液”),此时该硝酸钾溶液的溶质质量分数是28.6%(保留一位小数).
(5)实验室中,盐酸和氢氧化钠的中和反应后的溶液中含有氯化钠.某同学将10.0g稀盐酸滴加到溶质质量分数是10.0%的氢氧化钠溶液8.0g中(含2滴酚酞试液),混合液刚好由红色变为无色时可认为恰好完全反应,求:
①所用盐酸中溶质的质量.(计算结果精确到0.01g)
②保持温度为20℃,将反应后的氯化钠的不饱和溶液变成饱和溶液,根据计算写出一种可行的方法.(计算结果精确到0.1g)
15.春节是中华民族的传统节日,下列相关活动涉及化学变化的是( )
| A. |  贴春联 贴春联 | B. |  剪窗花 剪窗花 | C. |  燃爆竹 燃爆竹 | D. |  包饺子 包饺子 |
19. 根据氯化钠和硝酸钾的溶解度表,回答下列问题:
根据氯化钠和硝酸钾的溶解度表,回答下列问题:
(1)在20℃时,将50克氯化钠溶解到100克水中,形成的溶液的溶质质量分数为26.5%;
(2)当硝酸钾中混有少量氯化钠时,提纯硝酸钾所采用的方法是降温结晶;
(3)如图所示,小烧杯中盛放硝酸钾溶液,底部有少量未溶解的硝酸钾晶体,若将氢氧化钠固体投入到大烧杯的水中,不断搅拌,则小烧杯底部硝酸钾晶体的质量将减小(选填“增大”、“减小”或“不变”).
 根据氯化钠和硝酸钾的溶解度表,回答下列问题:
根据氯化钠和硝酸钾的溶解度表,回答下列问题:| 名称 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ |
| 氯化钠 | 35.8g | 36.0g | 36.3g | 36.6g | 37.0g | 37.3g | 37.8g |
| 硝酸钾 | 20.9g | 31.6g | 45.8g | 63.9g | 85.5g | 110g | 138g |
(2)当硝酸钾中混有少量氯化钠时,提纯硝酸钾所采用的方法是降温结晶;
(3)如图所示,小烧杯中盛放硝酸钾溶液,底部有少量未溶解的硝酸钾晶体,若将氢氧化钠固体投入到大烧杯的水中,不断搅拌,则小烧杯底部硝酸钾晶体的质量将减小(选填“增大”、“减小”或“不变”).
20.下列对物质的溶解性的描述中,错误的是( )
| A. | 物质的溶解性有强有弱,强弱不同 | |
| B. | 在一定条件下,一定量的水中,物质不能够无限的溶解 | |
| C. | 溶解性大小只与物质的性质有关,跟其他因素无关 | |
| D. | 物质的溶解性是指一种物质在另一种物质中的溶解能力 |
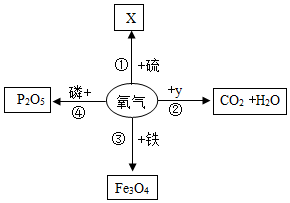 氧气能与许多物质发生反应.小明同学学习了之后进行了如图整理.(部分反应条件已略去).
氧气能与许多物质发生反应.小明同学学习了之后进行了如图整理.(部分反应条件已略去).