题目内容
17.如图1是实验室常用的实验装置,请回答有关问题: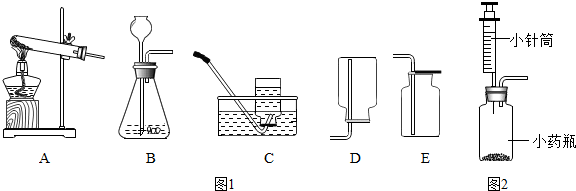
(1)装置C由导管、水槽和集气瓶(填仪器的名称)组成.
(2)实验室用KClO3制取O2时的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,实验室可以用B装置来制备CO2请写出化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑
(3)氨气(NH3)是一种密度比空气小,极易溶于水的气体,实验室可用加热氯化铵和氢氧化钙固体混合物制得氨气.制取与收集氨气应选择A和D装置.(填序号)
(4)小红用家里的小针筒和废药瓶组装成一套微型装置(如图2所示)替代装置B,得到老师的表扬,用该装置做实验的优点是①③ (填序号).
①节约药品用量 ②能完全消除废液排放
③能控制液体的滴加速度 ④产生的气体不含任何杂质.
分析 (1)根据实验室常用仪器解答;
(2)根据氯酸钾与二氧化锰制氧气时会生成氯化钾和氧气;石灰石与盐酸反应制取二氧化碳时会生成氯化钙、水和二氧化碳;
(3)实验室可用加热氯化铵和氢氧化钙固体混合物制得氨气解答.
(4)装置改进后的优点是:操作简便;节约药品用量;能控制液体的滴加速度,从而能够控制反应的进行.
解答 解:
(1)仪器名称为:水槽、集气瓶
(2)氯酸钾与二氧化锰制氧气时会生成氯化钾和氧气,二氧化锰是催化剂,故化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;石灰石与盐酸反应制取二氧化碳时会生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)实验室可用加热氯化铵和氢氧化钙固体混合物制得氨气,故选用固体加热装置作为发生装置;氨气(NH3)是一种密度比空气小,极易溶于水的气体,故只能选用向下排空气法收集;
(4)装置改进后的优点是:操作简便;节约药品用量;能控制液体的滴加速度,从而能够控制反应的进行.故答案为:①③.
故答案为:
(1)水槽 集气瓶
(2)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ CaCO3+2HCl═CaCl2+H2O+CO2↑
(3)A D
(4)①③
点评 本题考查常见气体的制取实验和相关问题,属于基础知识类问题,只要同学们能够细心,做好此题不难.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
5.化学兴趣小组对“影响金属与盐酸反应剧烈程度的因素”进行了探索.
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】a、可能与金属本身的性质有关
b、可能与盐酸的浓度有关
c、…
【活动探究1】为探究猜想a,分别在两支试管中放入相同质量的锌片和铁片(所用金属均已用砂纸打磨),然后分别加入相同尝试和质量的稀盐酸,
(1)观察到放锌片的试管中立即产生大量气泡,发生反应的化学方程式是Zn+2HCl═ZnCl2+H2↑.
(2)放铁片的试管中只产生少量气泡,溶液由无色变为浅绿色.
(3)从实验现象可判断:金属活动性Zn>Fe(填“<”“=”“>”).
(4)得出结论:金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是金属的活动性越强,与相同的盐酸反应越剧烈.
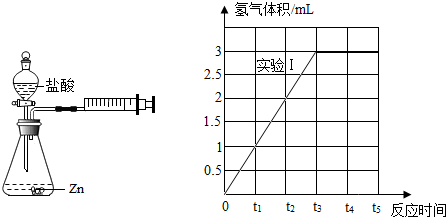
【活动探究2】为探究猜想b,设计如图的装置进行实验,其中注射器用于测量产生氢气的体积.
所用药品,实验数据如表(盐酸足量):
(5)请在坐标图中画出实验编号Ⅱ产生氢气与时间的关系图.
(6)得出结论:金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是相同条件下,盐酸的浓度越大,金属与盐酸反应越快(“块”或“慢”).
(7)通过以上探究,你认为金属与盐酸反应的剧烈程度可能还受哪些因素的影响温度(写一条即可).
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】a、可能与金属本身的性质有关
b、可能与盐酸的浓度有关
c、…
【活动探究1】为探究猜想a,分别在两支试管中放入相同质量的锌片和铁片(所用金属均已用砂纸打磨),然后分别加入相同尝试和质量的稀盐酸,
(1)观察到放锌片的试管中立即产生大量气泡,发生反应的化学方程式是Zn+2HCl═ZnCl2+H2↑.
(2)放铁片的试管中只产生少量气泡,溶液由无色变为浅绿色.
(3)从实验现象可判断:金属活动性Zn>Fe(填“<”“=”“>”).
(4)得出结论:金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是金属的活动性越强,与相同的盐酸反应越剧烈.
【活动探究2】为探究猜想b,设计如图的装置进行实验,其中注射器用于测量产生氢气的体积.
所用药品,实验数据如表(盐酸足量):
| 实验编号 | 选用金属(质量形状相同) | 盐酸浓度(相同体积) | 产生氢气的体积/mL | |||||
| 0 | t1 | t2 | t3 | t4 | t5 | |||
| Ⅰ | 锌片 | 6% | 0 | 1 | 2 | 3 | 3 | 3 |
| Ⅱ | 锌片 | 3% | 0 | 0.6 | 1.2 | 1.8 | 2.4 | 3 |
(6)得出结论:金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是相同条件下,盐酸的浓度越大,金属与盐酸反应越快(“块”或“慢”).
(7)通过以上探究,你认为金属与盐酸反应的剧烈程度可能还受哪些因素的影响温度(写一条即可).

12.2013年5月,我市研发出7μm超薄铜箔,该项技术全国领先.铜能加工成铜箔是利用铜的( )
| A. | 导电性 | B. | 延展性 | C. | 可燃性 | D. | 抗腐蚀性 |
2.生活中许多变化都能产生热量,下列放热现象主要是由物理变化引起的是( )
| A. | 木炭燃烧放热 | B. | 生石灰与水混合放热 | ||
| C. | 电暖宝通电发热 | D. | 苹果腐烂发热 |
9.实验室科学探究的重要手段,下列化学实验操作不正确的是( )
| A. |  液体的倾倒 | B. | 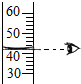 液体的量取 | C. | 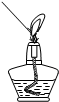 点燃酒精灯 | D. |  滴加液体 |

 回答下列问题:
回答下列问题: