题目内容
17.白钨矿(主要成分为CaWO4)中钨元素(W)的化合价是( )| A. | +6 | B. | +4 | C. | +2 | D. | -2 |
分析 根据在化合物中正负化合价代数和为零,结合CaWO4化学式进行解答本题.
解答 解:钙元素显+2价,氧元素显-2价,设钨元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+2)+x+(-2)×4=0,则x=+6价.
故选:A.
点评 本题难度不大,掌握利用化合价的原则(化合物中正负化合价代数和为零)计算指定元素的化合价的方法即可正确解答本题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.下列不能由金属和酸直接反应得到的物质是( )
| A. | 硫酸铜 | B. | 硫酸锌 | C. | 氯化亚铁 | D. | 氯化镁 |
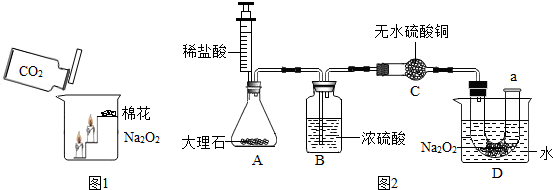
2.空气是人类活动必需的自然资源.工业上常用分离空气的方法制取氧气,如图1所示,实验室常用物质分解的方法制取氧气.

(1)写出标有序号的仪器名称:a分液漏斗,b集气瓶.
(2)在实验室中用过氧化氢溶液和二氧化锰混合制取并收集氧气,可选择BC或BE装置(填字母代号).
(3)学习了MnO2对过氧化氢分解有催化作用的知识后.某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了如下探究.
【猜想】Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后质量和化学性质都不变.
【实验】用天平称量0.2g CuO,取5mL 5%过氧化氢溶液于试管中,进行如图2实验:

(一)填表:
(二)步骤①的目的是与②进行对比;
(三)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒;
(四)过氧化氢能被CuO催化分解放出O2的化学方程式为2H2O2$\frac{\underline{\;氧化铜\;}}{\;}$2H2O+O2↑.
【拓展】要探究步骤⑤做过催化剂的CuO其它化学性质,还应补做的实验是用氢气(或一氧化碳或炭)还原固体,观察固体是否变成红色;或用加热的稀硫酸溶液固体,观察是否能生成蓝色溶液.

(1)写出标有序号的仪器名称:a分液漏斗,b集气瓶.
(2)在实验室中用过氧化氢溶液和二氧化锰混合制取并收集氧气,可选择BC或BE装置(填字母代号).
(3)学习了MnO2对过氧化氢分解有催化作用的知识后.某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了如下探究.
【猜想】Ⅰ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后质量和化学性质都不变.
【实验】用天平称量0.2g CuO,取5mL 5%过氧化氢溶液于试管中,进行如图2实验:

(一)填表:
| 步骤③现象 | 步骤⑥结果 | 结论 |
| 带火星的木条复燃 | 固体质量是0.2g | 猜想Ⅰ、Ⅱ不成立 猜想Ⅲ成立 |
(三)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒;
(四)过氧化氢能被CuO催化分解放出O2的化学方程式为2H2O2$\frac{\underline{\;氧化铜\;}}{\;}$2H2O+O2↑.
【拓展】要探究步骤⑤做过催化剂的CuO其它化学性质,还应补做的实验是用氢气(或一氧化碳或炭)还原固体,观察固体是否变成红色;或用加热的稀硫酸溶液固体,观察是否能生成蓝色溶液.
6.下列实验操作正确的是( )
| A. | 排水法收集氧气时,当导管口能开始有气泡冒出时立即收集,防止气体逃逸 | |
| B. | 稀释浓硫酸时,沿烧杯壁将水缓缓注入盛有浓硫酸的烧杯中,并用玻璃棒不断搅拌 | |
| C. | 过滤时,用玻璃棒在过滤器中不断搅拌 | |
| D. | 氢气、一氧化碳等可燃性气体点燃前进行验纯 |
 能源是人类生存和发展的基础,能源成为人们日益关注的问题.
能源是人类生存和发展的基础,能源成为人们日益关注的问题.