题目内容
14.根据如图所示水、二氧化碳和氧气的性质实验,请回答以下问题.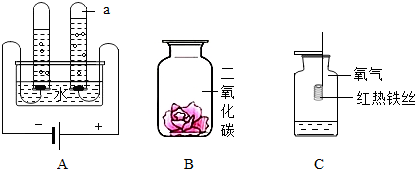
(1)仪器a的名称是试管A装置中发生反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
用带火星的木条检验a中的气体,观察到木条复燃,该气体是氧气.
(2)将用紫色石蕊试液浸泡过的纸花喷水后,放入集气瓶B中,观察到的现象是紫色小花变红,该反应的化学方程式是H2O+CO2=H2CO3.
(3)C中的铁丝要绕成螺旋状,其目的是增大铁丝与氧气的接触面积,该反应的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
分析 (1)根据反应物和生成物及其质量守恒定律可以书写化学方程式,氧气能使带火星的木条复燃;
(2)根据二氧化碳与水反应生成酸,显酸性的溶液能使石蕊试液变红色;
(3)根据铁丝在氧气中燃烧实验的注意事项和反应原理分析解答.
解答 解:(1)由装置图中仪器a可知a为试管;水在通电条件下反应生成氢气和氧气,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;氧气能使带火星的木条复燃,所以该气体为氧气;
(2)二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊试液变红,反应的化学方程式为:H2O+CO2=H2CO3;
(3)铁丝在氧气中燃烧实验中为了增大铁丝与氧气的接触面积,将铁丝绕成螺旋状,反应过程中生成四氧化三铁,反应的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
故答案为:(1)试管;2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;氧气;
(2)紫色小花变红;H2O+CO2=H2CO3;
(3)增大铁丝与氧气的接触面积;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
点评 解答本题要掌握化学方程式的书写方法,理解能使带火星的木条复燃的气体是氧气,理解二氧化碳的化学性质方面的知识,掌握铁在氧气中燃烧的实验现象及其反应的实质.

练习册系列答案
相关题目
5.常用于检验二氧化碳气体的物质是( )
| A. | 水 | B. | 澄清石灰水 | C. | 食盐水 | D. | 糖水 |
6.小华同学为测定石灰石中碳酸钙的质量分数,称取5.55克石灰石粉末,进行四次高温加热(杂质不反应),冷却后反复称量剩余固体,记录数据如表:
①完全反应生成二氧化碳5 克.
②石灰石中碳酸钙的质量分数为90.1%.(精确到0.1%)
③充分煅烧该石灰石20吨,可制得含杂质30%的生石灰多少吨?
| 次序 | 1 | 2 | 3 | 4 |
| 剩余固体质量 | 4.25 | 3.95 | 3.35 | 3.35 |
②石灰石中碳酸钙的质量分数为90.1%.(精确到0.1%)
③充分煅烧该石灰石20吨,可制得含杂质30%的生石灰多少吨?
4.制取氢气可使用启普发生器,它是一种随开随用随关随停的气体发生装置,下列各装置能与启普发生器产生相同效果的是( )


| A. | ①②③ | B. | ①④⑤ | C. | ①③⑤ | D. | 全部 |