题目内容
19.根据下列装置图,回答有关问题: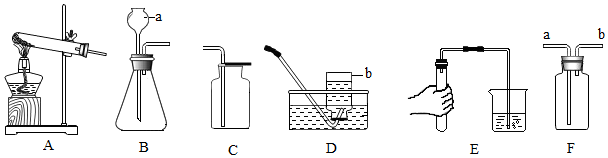
(1)图E的目的是检查装置气密性.
(2)写出实验室用加热氯酸钾和二氧化锰混合物制取氧气的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,可选择的装置组合是AC或AD(填字母),其基本反应类型是分解反应.
(3)若使用高锰酸钾制取氧气,可选用的发生装置是A(填字母),还需进行的改进地方是在试管口放一团棉花,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(4)丙同学用图F进行排空气法收集氧气,气体应从a(填“a”或“b”)端通入.
(5)常温下,硫化氢是一种有臭鸡蛋气味的有毒气体,密度比空气大,能溶于水.实验室可在常温下用硫化亚铁固体和稀硫酸反应生成硫化氢气体和硫酸亚铁.若制取硫化氢气体,从图中选择的实验装置是BC.
分析 (1)图E的目的是检查装置气密性;
(2)根据氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气,写出文字表达式和确定反应类型即可;根据反应物的状态和反应条件确定发生装置;根据氧气的密度比空气的密度大,不易溶于水选择收集装置即可;
(3)根据反应物的状态和反应条件确定发生装置;根据高锰酸钾制取氧气时的注意事项进行分析;根据高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气写出反应的化学方程式即可;
(4)根据氧气密度比空气大,应长管进入气体进行分析;
(5)根据反应物状态和反应条件选择发生装置,根据气体密度和溶解性选择收集装置.
解答 解:(1)图E的目的是检查装置气密性;
故填:检查装置气密性.
(2)实验室用加热氯酸钾和二氧化锰混合物制取氧气,氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气,该反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;该反应属于分解反应;因为反应需要加热,可选择的发生装置为A;因为氧气的密度比空气大,可以用向上排空气法收集,即用C装置收集,氧气不易溶于水,可以用排水法收集,即用D装置收集.
故填:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;AC或AD;分解反应;
(3)利用高锰酸钾制取氧气需要加热,应该用A装置作为发生装置;用加热高锰酸钾制氧气,试管口要有一团棉花,其作用是防止高锰酸钾粉末进入导管;高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
故填:A;在试管口放一团棉花;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(4)氧气密度比空气大,应从a端进入,将空气从b端排出;
故填:a;
(5)实验室用块状固体硫化亚铁(FeS)与稀硫酸在常温下反应制取硫化氢气体,反应物是固体,反应条件是常温,故发生装置选B,氯化氢气体密度比空气大,能溶于水,所以只能用向上排空气法收集,故收集装置选C;
故填:BC.
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

 天天向上口算本系列答案
天天向上口算本系列答案| X | Y | Z | ||||||||||
| ① | CO2 | Ca(OH)2溶液 | H2O | |||||||||
| ② | CO | Fe2O3 | C | |||||||||
| ③ | 稀盐酸 | 大理石 | Na2CO3 | |||||||||
| ④ | O2 | CH4 | P | |||||||||
| A. | ①② | B. | ①③ | C. | ①③④ | D. | ①②③④ |
| A. | 生成2.0 gCO2气体 | B. | 原来CaCO3为12.5 g | ||
| C. | 生成了5.6 gCaO | D. | 剩余CaCO3为3.0 g |
 如图,小新同学将学校荷花池中浑浊的水样倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿,采用如图的装置进行过滤.加明矾的作用是加速沉降.图中缺少的一种仪器是玻璃棒,其作用是引流;
如图,小新同学将学校荷花池中浑浊的水样倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿,采用如图的装置进行过滤.加明矾的作用是加速沉降.图中缺少的一种仪器是玻璃棒,其作用是引流; 根据下列装置图,回答有关问题:
根据下列装置图,回答有关问题:
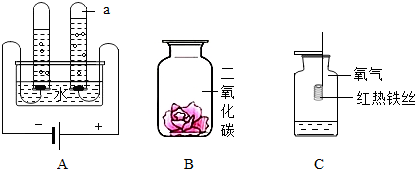

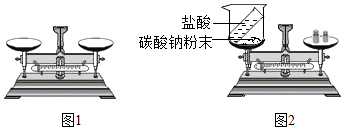 请根据题目要求回答下列问题.
请根据题目要求回答下列问题.