题目内容
18.归纳总结是学习化学的重要方法,小明同学总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应)如图1所示.
(1)为了验证反应①,小明将无色酚酞试液滴入NaOH溶液中,溶液变成红色.
(2)依据反应②说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为2NaOH+CO2=Na2CO3+H2O
(3)为了验证反应③能够发生,你选择的物质是C.
A、Na2CO3 B、HCl C、CuSO4 D、BaCl2.
(4)小明用微观示意图(如图2)来说明反应③的发生,用化学反应方程式表示为2NaOH+H2SO4=Na2SO4+2H2O
从该图中可以看出,反应后的溶液pH>7(填“>”、“<”或“=”)
分析 (1)根据酸碱指示剂遇到酸碱的变色进行分析;
(2)根据氢氧化钠会与空气中的二氧化碳反应进行分析;
(3)根据碱与盐的反应进行分析;
(4)根据微观图示中的微粒图示进行分析发生的反应及溶液的酸碱性.
解答 解:(1)碱溶液会使酚酞变红色.所以,将无色酚酞试液滴入NaOH溶液中,溶液变成红色.
(2)氢氧化钠和二氧化碳反应生成碳酸钠和水,其化学反应方程式为:2NaOH+CO2=Na2CO3+H2O;
(3)A、碳酸钠和氢氧化钠不满足复分解反应的条件,不反应,故A不符合题意;
B、盐酸是酸能与氢氧化钠发生中和反应,故B不符合题意;
C、硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,满足复分解反应的条件,是碱与盐的反应,故C符合题意;
D、氯化钡和氢氧化钠不满足复分解反应的条件,不反应,故D不符合题意;
(4)容器中是氢氧根离子和钠离子,加入的是硫酸根离子和氢离子,所以反应物是氢氧化钠和硫酸,生成物中有钠离子、硫酸根离子和水分子,所以生成物是硫酸钠和水,反应的方程式是:2NaOH+H2SO4=Na2SO4+2H2O.根据反应后的容器中有氢氧根离子,所以溶液显碱性,溶液的PH值大于7.
故答为:(1)红;(2)2NaOH+CO2=Na2CO3+H2O;(3)C;(4)2NaOH+H2SO4=Na2SO4+2H2O,>.
点评 在解此类题时,首先分析图示所表示的反应的实质,然后结合学过的知识和复分解反应的条件进行解答.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
9.A、B、C三种物质各5克组成的混合物放在密闭容器中加热后,A完全反应,C反应后质量为9克,生成2克新物质D,则该反应中A和B的质量比是( )
| A. | 5:1 | B. | 1:5 | C. | 1:4 | D. | 1:1 |
6.胆矾是一种蓝色晶体,受热时易失去结晶水,成为白色粉未;在工业上精炼铜、镀铜等过程中都需要胆矾.上述对胆矾的描述中.没有涉及到的是( )
| A. | 物理性质 | B. | 化学性质 | C. | 组成 | D. | 用途 |
10.化学用语是最简明、信息丰富、国际通用的语言.下列对化学用语解释不正确的是( )
| A. | 2S-2个硫原子 | B. | Na+-钠离子 | C. | H3-3个氢分子 | D. | N2-氮气 |
7.下列实验现象的描述中,错误的是( )
| A. | 铁丝在氧气中燃烧,火星四射,放出热量,生成黑色固体 | |
| B. | 纯净的氢气在空气中安静地燃烧,产生淡蓝色火焰,生成了水 | |
| C. | 铜绿中加入足量稀盐酸,有气泡产生,最终得到蓝色溶液 | |
| D. | 氨水中滴加几滴无色酚酞试液,溶液变成了红色 |
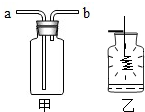 小科在实验室完成了氧气的制取并收集了一瓶氧气用来做铁丝在氧气中的燃烧实验.
小科在实验室完成了氧气的制取并收集了一瓶氧气用来做铁丝在氧气中的燃烧实验.



