题目内容
17.在杭州经济大开发的进程中,要坚持开发与环保并重.某化学课外活动小组在调查一化工厂时发现该厂有甲、乙两个车间,排出的废水澄清透明,经分析分别含有三种不同的离子,共有K+、Ba2+、Cu2+、OH-、NO3-、CO32-六种离子,经查部分物质的溶解性见下表:| OH- | NO3- | CO32- | |
| K+ | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 不 |
| Cu2+ | 不 | 溶 | 不 |
(2)已知甲车间废水明显呈碱性,则乙车间废水中含有的阴离子是NO3-.
(3)根据以上溶解性表判断,Cu(NO3)2和Ba(OH)2溶液能(填“能”或“不能”)发生复分解反应.若能反应写出化学方程式;若不能反应写出理由:Cu(NO3)2+Ba(OH)2═Cu(OH)2↓+Ba(NO3)2.
分析 根据复分解反应发生的条件可知若离子结合生成水、气体或沉淀时,离子不能共存在溶液中,由溶解性表可知Cu(OH)2↓、BaCO3↓、CuCO3↓,则Cu2+、OH-不能共存,Ba2+、Cu2+-、CO32-不能共存,则可判断两废水中的离子.
解答 解:(1)因共有K+、Ba2+、Cu2+、OH-、NO3-、CO32-六种离子,将甲、乙两车间的废水按适当的比例混合,能使废水中的Ba2+、Cu2+、OH-、CO32-等离子转化为沉淀除去,则清液中含有K+、NO3-,即溶质为KNO3,故答案为:KNO3.
(2)甲车间废水明显呈碱性,说明甲车间含有OH-和CO32-,Ba2+可以与CO32-结合成沉淀,Cu2+可以与OH-结合成沉淀,所以甲车间不含Ba2+和Cu2+,Ba2+和Cu2+应在乙车间,故乙车间的阴离子为NO3-,故答案为:NO3-;
(3)Cu(NO3)2和Ba(OH)2溶液中所含的铜离子可以与钡离子结合成沉淀,故能发生复分解反应,故答案为:能,Cu(NO3)2+Ba(OH)2═Cu(OH)2↓+Ba(NO3)2.
点评 本题以工业生产中的废水处理来考查复分解反应发生的条件,具有较强的实际应用性,在考查学生解决问题的能力上有实际价值,学生应熟记反应的条件及明确物质的溶解性表的作用并学会正确利用.

练习册系列答案
相关题目
16.如图所示实验得出的结论,不正确的是( )
| A. |  呼出气体中CO2含量比吸入空气中CO2含量高 | |
| B. |  蜡烛中含氢元素 | |
| C. |  红热的铁丝在氧气中能燃烧 | |
| D. |  水是由氢、氧元素组成的 |
5.图为A、B、C三种固体物质(不含结晶水)的溶解度曲线.下列说法错误的是( )
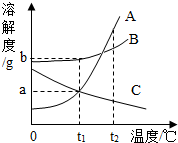

| A. | t1℃时,三种物质中B的溶解度最大 | |
| B. | t2℃时,取三种物质各a g分别放入100g水中充分溶解,只有C物质能形成饱和溶液 | |
| C. | 将等质量的三种物质的饱和溶液分别由t2℃降温到t1℃,A溶液中析出的晶体质量最大 | |
| D. | 可用降温的方法使接近饱和的C溶液变为饱和溶液 |
2.归纳总结是学习化学一种常用的方法.下列归纳总结中说法正确的是( )
①水银不是银,而是金属汞,常温常压下是液态,有毒;②铅笔芯中不含铅,主要是石墨和粘土;③干冰不是冰,而是固体二氧化碳 ④纯碱不是碱,而是一种盐.
①水银不是银,而是金属汞,常温常压下是液态,有毒;②铅笔芯中不含铅,主要是石墨和粘土;③干冰不是冰,而是固体二氧化碳 ④纯碱不是碱,而是一种盐.
| A. | ①②③④ | B. | ①②③ | C. | ②③④ | D. | ①③④ |
9.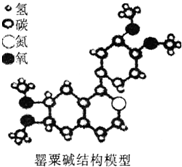 毒品是全球性公害,是人类共同的敌人.罂粟碱即是其中的一种,从组成和结构认识罂粟碱叙述正确的是( )
毒品是全球性公害,是人类共同的敌人.罂粟碱即是其中的一种,从组成和结构认识罂粟碱叙述正确的是( )
 毒品是全球性公害,是人类共同的敌人.罂粟碱即是其中的一种,从组成和结构认识罂粟碱叙述正确的是( )
毒品是全球性公害,是人类共同的敌人.罂粟碱即是其中的一种,从组成和结构认识罂粟碱叙述正确的是( )| A. | 罂粟碱是由四种原子构成的有机物 | |
| B. | 罂粟碱分子中含有4种原子 | |
| C. | 罂粟碱中氮、氧元素的质量比为1:4 | |
| D. | 罂粟碱中氢原子与碳原子的个数比为19:21 |

 化学反应遵循质量守恒定律.
化学反应遵循质量守恒定律.