题目内容
20.硫酸与氢氧化钠可发生如下的反应:2Na0H+H2S04═Na2SO4+2H2O.在50g的稀硫酸中加入4g氢氧化钠固体,恰好完全反应,则该硫酸中溶质的质量分数是多少?分析 根据题意,由参加反应的氢氧化钠的质量,由反应的化学方程式,列式计算出参加反应的硫酸的质量,进而计算出该硫酸中溶质的质量分数.
解答 解:设参加反应的硫酸中溶质的质量是x
2Na0H+H2S04═Na2SO4+2H2O
80 98
4g x
$\frac{80}{98}=\frac{4g}{x}$ x=4.9g
该硫酸中溶质的质量分数为$\frac{4.9g}{50g}$×100%=9.8%.
答:该硫酸中溶质的质量分数为9.8%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
10.我们知道物质有多种不同的分类方法,下列各组化合物中按某一条件,属于同一类的是( )
| A. | H2O、CaO、KClO3 | B. | KCl、KOH、KClO3 | ||
| C. | CO、CO2、H2CO3 | D. | CH4、聚乙烯塑料、顺丁橡胶 |
11.下列物质之间,不存在如图所示转化关系的是(“→”表示能转化)( )
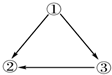

| A. | ①H2O2 ②H2O ③O2 | B. | ①Na2CO3 ②CO2 ③CaCO3 | ||
| C. | ①Ca(OH)2 ②CaCO3 ③NaOH | D. | ①O2 ②H2O ③CuO |
8.下列有关化学符号“H2O”表示的意义,错误的是( )
| A. | 水这种物质 | |
| B. | 一个水分子由两个氢原子和一个氧原子构成 | |
| C. | 一个水分子中含有一个氢分子 | |
| D. | 水由氢元素和氧元素组成 |
12.铝合金是工业中应用最广泛的一类有色金属结构材料,在航空、航天、汽车、机械制造、船舶及化学工业中已大量应用.工业经济的飞速发展,对铝合金的需求日益增多,使铝合金的研究也随之深入.已知某合金粉末除铝外,还含有铁、铜中的一种或两种.某兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究.
查阅资料:铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有铜(填名称).
猜想3:该合金粉末中除铝外,还含有铁、铜.
实验探究:下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
探究结论:猜想3成立.
反思:一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.写出铝与稀盐酸反应的化学方程式2Al+6HCl═2AlCl3+3H2↑.
查阅资料:铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有铜(填名称).
猜想3:该合金粉末中除铝外,还含有铁、铜.
实验探究:下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的30% NaOH溶液,充分反应后过滤,滤渣备用. | 粉末部分溶解,并有气体放出. | 合金中一定含有铝. |
| ②取步骤①所得滤渣,加过量的10% 盐酸,充分反应. | 滤渣部分溶解,并有气体放出,溶液呈浅绿色. | 合金中一定含有铁和铜. |
反思:一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.写出铝与稀盐酸反应的化学方程式2Al+6HCl═2AlCl3+3H2↑.
 ”、“
”、“ ”、“
”、“ ”表示核电荷数不同的原子,其中能用来表示混合物的是①C;能表示3H2的是②B(填图下字母,下同)能用来表示氧化物的是③A.能用来表示铁这种物质的是④D.
”表示核电荷数不同的原子,其中能用来表示混合物的是①C;能表示3H2的是②B(填图下字母,下同)能用来表示氧化物的是③A.能用来表示铁这种物质的是④D.
 甲、乙两个装置均可用于证明SO2易溶于水.
甲、乙两个装置均可用于证明SO2易溶于水.