题目内容
14.下面是实验室制取和收集气体的装置,请按要求作答: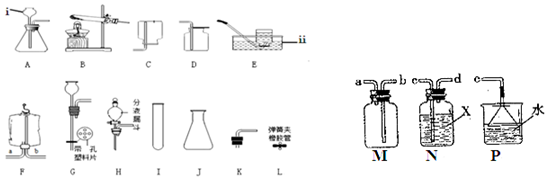
(1)写出仪器的名称:ⅰ长颈漏斗、ⅱ水槽.
(2)若选择B、D组合一套装置制取氧气,请写出有关反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;若用装置D收集O2,验满的方法是用带火星的木条放在集气瓶口,如果木条复燃,证明集气已集满.相对D而言,收集氧气选用装置E的优点是收集到的气体更纯.使用E装置收集氧气,应注意气泡连续均匀冒出时开始收集.
(3)实验室可用稀硫酸和锌粒在常温下反应制取氢气,应选A-E中的A作为发生装置.若用图F所示的医用塑料袋排空气法收集H2,则H2导入端为b(填“a”或“b”).
(4)小丽用H2O2和MnO2制取O2,若用HJK组合,优点是可以控制反应速率.若想用以上仪器组装一个可随时使反应发生或停止的发生装置,她应选G-L中的GIL进行组合.
(5)SO2是一种无色有刺激性气味的有毒气体,密度比空气大,易溶于水,排放到空气中会形成酸雨.实验室用图M、N、P装置收集一瓶干燥的SO2,(提示:X内装的是浓硫酸,起干燥气体的作用).则M、N、P的接口连接顺序是cdbae.
分析 (1)根据仪器的名称进行解答;
(2)根据高锰酸钾受热分解产生了锰酸钾、二氧化锰和氧气写出反应的化学方程式即可;根据氧气的助燃性进行分析;根据用排水法收集的氧气更纯净进行分析;根据排水法收集氧气的注意事项进行分析;
(3)根据锌粒和稀硫酸在常温下制取氢气,属于固液常温型选择发生装置即可;根据氢气的密度比空气小进行分析;
(4)根据实验的要求及装置特点分析;
(5)根据SO2的性质、实验要求及装置特点进行分析.
解答 解:(1)图中所示仪器是:ⅰ是长颈漏斗,ⅱ是水槽;
(2)因为A图中有棉花,故用高锰酸钾制氧气,用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,因此反应的化学方程式为:2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑;检验氧气是否集满的方法是利用氧气的助燃性,用带火星的木条放在集气瓶口,如果复燃,证明集气瓶内已充满氧气;用排水法收集的氧气更纯净,排水法收集氧气的最佳时刻是等气泡连续均匀冒出时开始收集;
(3)锌粒和稀硫酸在常温下制取氢气,属于固液常温型,故选A;若用图F所示的医用塑料袋排空气法收集H2,因为氢气的密度比空气小,故氢气从长管进入到医用塑料袋的上方,把空气从短管排出,则H2导入端为b;
(4)若用HJK组合制取氧气时,可利用分液漏斗控制滴加液体的速度,从而达到控制反应速率的目的;若组装一个可随时使反应发生或停止的发生装置,应选GIL组合进行实验,这样需要终止反应时,可用弹簧夹夹住橡皮管,锥形瓶内气压升高把液体压入长颈漏斗,从而使固液反应物分离,达到终止反应的目的;
(5)装置的导管按气流方向连接的顺序是:通过c导管把二氧化硫导入试剂瓶中进行干燥,通过d导管导出后,通过b导管导入集气瓶中收集,为了防止二氧化硫逸出扩散到空气中污染环境,应该把a导管连接到e导管上,通过水吸收逸出的二氧化硫;
故答案为:(1)长颈漏斗;水槽; (2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;用带火星的木条放在集气瓶口,如果木条复燃,证明集气已集满;收集到的气体更纯;气泡连续均匀冒出;(3)A;b;(4)可以控制反应速率;GIL;(5)cdbae.
点评 本题考查了常见气体发生装置和收集装置的选择,制取气体的反应原理、步骤、注意事项等知识,完成此题,可以依据已有的知识进行.要求同学们在完成此类题目时,要熟知反应物的状态和反应的条件以及气体的密度和水溶性,以便做出正确的判断.

| A. | 若试管外壁有水珠,加热前一定要擦干 | |
| B. | 加热时,试管口一定要对着他人 | |
| C. | 给试管里的药品加热,一定要先进行预热 | |
| D. | 用试管夹夹持试管加热,应夹在距试管口$\frac{1}{3}$处 |







 用推拉注射器活塞的方法可以检查图中装置的气密性.
用推拉注射器活塞的方法可以检查图中装置的气密性.