题目内容
9.质量守恒定律的定量研究对化学科学发展具有重大意义.(1)我国从今年5月1日起酒驾入刑.“酒精检测仪”可检查司机是否酒后驾车,其反应原理为C2H5OH+4CrO3+6H2SO4═2Cr2(SO4)3+2CO2↑+9X,反应中红色的CrO3转变为绿色的Cr2(SO4)3,其中X的化学式为CO2.
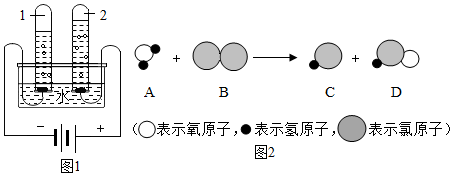
(2)A、B、C、D表示四种物质,其微观示意图见下表,A和B在一定条件下反应生成C和D,若16gB参加反应,则生成D的质量为18g.
| 物质 | A | B | C | D |  |
| 微观示意图 |  |  |  |  |
分析 (1)根据反应前后原子的种类和数目不变来进行判断X的化学式;
(2)根据图示写出化学方程式即可解答.
解答 解:(1)根据质量守恒定律,反应前后原子种类和个数都不变,由方程式知反应物中含有的原子种类及原子个数为C:2;H:18;Cr:4;O:37;S:6;已知生成物中含有的原子种类及原子个数为H:18;Cr:4;O:33;S:6;比较分析可知X中含有C和O元素,其原子个数分别为2,4;故X的化学式为CO2.
故填:CO2.
(2)据图可知反应的化学方程式为:2H2S+O2═2S+2H2O.
B是氧气,D是水,质量比为8:9,若16gB参加反应,则生成D的质量:18g;
故填:18.
点评 本题主要考查学生对质量守恒定律的认识和灵活运用这一定律解答问题的能力,质量守恒定律适用于所有的化学变化.

练习册系列答案
相关题目
20. 如图装置常用来测定空气中氧气的含量.下列对该实验的认识中正确的是( )
如图装置常用来测定空气中氧气的含量.下列对该实验的认识中正确的是( )
 如图装置常用来测定空气中氧气的含量.下列对该实验的认识中正确的是( )
如图装置常用来测定空气中氧气的含量.下列对该实验的认识中正确的是( )| A. | 红磷燃烧后立即打开止水夹 | |
| B. | 燃烧匙中的红磷可以换成细铁丝 | |
| C. | 该实验可说明N2难溶于水 | |
| D. | 红磷的量不足会导致进入集气瓶中水的体积大于$\frac{1}{5}$ |
17.往800g溶质质量分数为10%的氢氧化钠溶液中通入一定量的二氧化碳,当生成两种盐的质量相等时,反应消耗二氧化碳的总质量约是(提示:Na2CO3+CO2+H2O═2NaHCO3)( )
| A. | 44g | B. | 61g | C. | 66g | D. | 72g |
4.区分日常生活中的下列物质,所用方法不完全正确的是( )
| 需鉴别的物质 | 方法1 | 方法2 |
| A、一氧化碳和二氧化碳 | 分别通入澄清石灰水 | 分别通过灼热的氧化铜 |
| B、铁粉和木炭粉 | 看颜色 | 用磁铁吸引 |
| C、硬水和蒸馏水 | 加肥皂水 | 分别蒸干 |
| D、黄金和黄铜 | 分别加热 | 分别加入稀硫酸 |
| A. | A | B. | B | C. | C | D. | D |
18.下面说法正确的是( )
| A. | 取块状固体时可以用镊子或者纸槽 | B. | 空气中氧气的质量分数约为21% | ||
| C. | 氙气可以用作照相机的闪光灯 | D. | 试管、烧杯、量筒都可以用来加热 |