题目内容
3.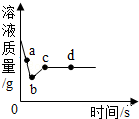 向一定质理AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间变化的情况如图所示.
向一定质理AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间变化的情况如图所示.(1)a点溶液中的溶质有AgNO3、Cu(NO3)2、Zn(NO3)2.
(2)图标上b~c段质量增加的原因是锌和硝酸铜反应生成硝酸锌和铜.
(3)d点溶液中溶质Zn(NO3)2(填化学式).
分析 锌和硝酸银反应生成硝酸锌和银;
锌和硝酸铜反应生成硝酸锌和铜.
解答 解:向一定质理AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉时,锌先和硝酸银反应生成硝酸锌和银,反应过程中溶液质量减小,当硝酸银完全反应后,锌再和硝酸铜反应生成硝酸锌和铜,反应过程中,溶液质量增大;
(1)a点溶液中的溶质有没有反应的硝酸银,反应生成的硝酸锌和没有反应的硝酸铜.
故填:AgNO3、Cu(NO3)2、Zn(NO3)2.
(2)图标上b~c段质量增加的原因是锌和硝酸铜反应生成硝酸锌和铜,随着反应的进行,溶液质量增大.
故填:锌和硝酸铜反应生成硝酸锌和铜.
(3)d点溶液中溶质只有硝酸锌.
故填:Zn(NO3)2.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
13.下列做法正确的是( )
| A. | 将浓盐酸露置于空气中 | B. | 加热除去纯碱变质后的产物 | ||
| C. | 消石灰与铵态氮肥共同施用 | D. | 用熟石灰鉴别CO(NH2)2与KCl |
14.某学生测定的下列数据中,不合理的是( )
| A. | 用pH试纸测得某地水的pH为6.1 | |
| B. | 用50ml的量筒量取了47.5ml的水 | |
| C. | 用托盘天平称得某粗盐的质量为21.4g | |
| D. | 测得某化肥尿素[CO(NH2)2]中的氮元素的质量分数为45% |
8.燃放烟花爆竹是我国春节的一项传统习俗,烟花点燃后绽放出的鲜艳夺目,五彩缤纷的图案是一些金属离子魅力的展示.焰火的主要原料是黑火药,还有草酸钠、碳酸铜(发出绿色的光)等发色剂和氯酸钾、金属镁、铝粉末等添加剂.下列说法正确的是( )
| A. | 碳酸铜因为受热分解才发出绿色的光 | |
| B. | 氯酸钾的主要用途是产生紫色的焰火 | |
| C. | 镁、铝在焰火中发出耀眼的白光 | |
| D. | 黑火药是我国古代的发明之一 |
13.下列有关水和空气的认识正确的是( )
| A. | 空气是一种宝贵的自然资源,由氮气和氢气组成 | |
| B. | 化石燃料的大量使用会导致大气中的氧气耗尽 | |
| C. | 用活性炭可以除去水中的异味和色素 | |
| D. | 水是最常用的溶剂,可以用水除去衣服上的油污 |

 某中学化学兴趣小组按照图甲的实验方法,做木炭粉与氧化铜反应实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现.他们决定对这个实验进行探究和改进.
某中学化学兴趣小组按照图甲的实验方法,做木炭粉与氧化铜反应实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现.他们决定对这个实验进行探究和改进. ,Mg原子在化学反应中容易失去(填“得到”或“失去”)2个电子.
,Mg原子在化学反应中容易失去(填“得到”或“失去”)2个电子.