题目内容
12.生活中处处有化学,通过学习已经知道:(1)“火碱”指的是(填化学式)NaOH;
(2)可用于洗涤油污的Na2CO3水溶液呈碱性(填“酸性”、“碱性”或“中性”);
(3)活性炭作为家用冰箱除味剂,是因为它具有吸附作用;
(4)NH4NO3(硝铵的主要成分)和(NH4)2SO4(肥田粉的主要成分)均属于盐(填“酸”“碱”或“盐”).
分析 (1)根据物质的化学式写法来分析;
(2)根据碳酸钠俗称纯碱,其水溶液显碱性,进行分析解答.
(3)根据活性炭具有吸附性,能吸附异味和色素,进行分析解答.
(4)根据NH4NO3和(NH4)2SO4的组成分析类别.
解答 解:(1)火碱是氢氧化钠的俗称,其化学式为NaOH;故填:NaOH;
(2)可用于洗涤油污的Na2CO3,俗称纯碱,其水溶液显碱性.故答案为:碱性.
(3)活性炭具有吸附性,能吸附异味和色素,则活性炭作为家用冰箱除味剂,是因为它具有吸附作用.故答案为:吸附.
(4)NH4NO3(硝铵的主要成份)和(NH4)2SO4(肥田粉的主要成分),都是由铵根离子和酸根粒子构成的化合物,属于均属于盐.故填:盐.
点评 本题主要考查了与生活中的化学知识,难度不大,加强化学知识的学习,解决好生活中的一些问题.

练习册系列答案
相关题目
2.下列实验现象的描述正确的是( )
| A. | 铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 | |
| B. | 硫在空气中燃烧,发出明亮的蓝紫色火焰,生成无色无味的气体 | |
| C. | 在电解水实验中,正负两极产生的气体体积比约为2:1 | |
| D. | 在如图所示试管中加入固体氢氧化钠,会发现红墨水右侧液面上升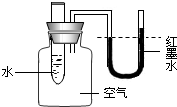 |
7.同学们对制作糕点常用膨松剂Na2CO3或NaHCO3进行了下列探究.
【查阅资料】
表1
表2
【探究一】NaHCO3和Na2CO3性质差异的探究
(1)现有20℃时溶质质量分数为8%的Na2CO3和NaHCO3溶液酸碱性:取样于试管中,分别滴加紫色石蕊试液,均显蓝色;酸碱度:NaHCO3溶液<Na2CO3溶液(填“>”或”“<”).
(2)稳定性:按图1,实验中可观察乙烧杯中的石灰水变浑浊,对应试管中发生反应的化学方程式为:
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
结论:在受热条件下,碳酸钠比碳酸氢钠稳定性强(填“强”或“弱”).
(3)利用溶解度鉴别NaHCO3和Na2CO3:分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察溶解现象来区分,X可以是下列的A.(选填A、B或C)
A.2g B.0.96g C.0.5g
【问题讨论】
(4)实验结束时,应先B(选填A或B).
A.熄灭酒精灯 B.将甲、乙烧杯移开
(5)甲认为探究稳定性实验中,由于受热时两物质温度不同,不能得到(2)中的结论,经对装置设计讨论后一致认为可以得到上述结论,理由是碳酸氢钠的受热温度低于碳酸钠的受热温度.
【探究二】测定NaHCO3和Na2CO3混合物10.0g中NaHCO3的质量分数(图2,夹持装置略)
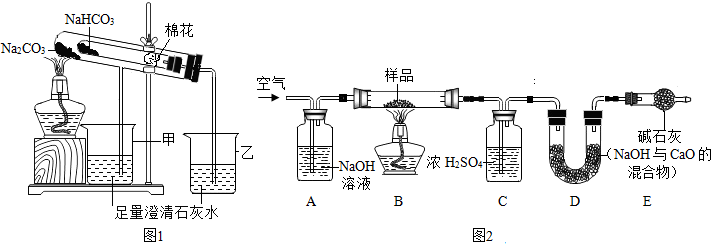
【问题讨论】
(6)实验前先通一段时间的空气的目的是把装置中的二氧化碳排尽;
(7)A的作用是吸收空气中的二氧化碳,若没有装置E,NaHCO3的质量分数测定结果会偏大(填“偏大”、“不变”或“偏小”).
(8)停止加热后,仍继续通入空气一段时间,目的是把反应生成的二氧化碳完全排入D中.
【含量测定】
(9)测得装置D的质量实验前为122.2g,实验后为124.4g,计算该样品中NaHCO3的质量分数.(要有计算过程)
【知识拓展】
(10)向Na2CO3溶液中通入CO2气体可以生成NaHCO3,该反应的化学反应方程式为:Na2CO3+CO2+H2O=2NaHCO3.
【查阅资料】
表1
| 20℃ | 8%Na2CO3溶液 | 8%NaHCO3溶液 |
| pH | 10.6 | 8.0 |
| 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
(1)现有20℃时溶质质量分数为8%的Na2CO3和NaHCO3溶液酸碱性:取样于试管中,分别滴加紫色石蕊试液,均显蓝色;酸碱度:NaHCO3溶液<Na2CO3溶液(填“>”或”“<”).
(2)稳定性:按图1,实验中可观察乙烧杯中的石灰水变浑浊,对应试管中发生反应的化学方程式为:
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
结论:在受热条件下,碳酸钠比碳酸氢钠稳定性强(填“强”或“弱”).
(3)利用溶解度鉴别NaHCO3和Na2CO3:分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察溶解现象来区分,X可以是下列的A.(选填A、B或C)
A.2g B.0.96g C.0.5g
【问题讨论】
(4)实验结束时,应先B(选填A或B).
A.熄灭酒精灯 B.将甲、乙烧杯移开
(5)甲认为探究稳定性实验中,由于受热时两物质温度不同,不能得到(2)中的结论,经对装置设计讨论后一致认为可以得到上述结论,理由是碳酸氢钠的受热温度低于碳酸钠的受热温度.
【探究二】测定NaHCO3和Na2CO3混合物10.0g中NaHCO3的质量分数(图2,夹持装置略)

【问题讨论】
(6)实验前先通一段时间的空气的目的是把装置中的二氧化碳排尽;
(7)A的作用是吸收空气中的二氧化碳,若没有装置E,NaHCO3的质量分数测定结果会偏大(填“偏大”、“不变”或“偏小”).
(8)停止加热后,仍继续通入空气一段时间,目的是把反应生成的二氧化碳完全排入D中.
【含量测定】
(9)测得装置D的质量实验前为122.2g,实验后为124.4g,计算该样品中NaHCO3的质量分数.(要有计算过程)
【知识拓展】
(10)向Na2CO3溶液中通入CO2气体可以生成NaHCO3,该反应的化学反应方程式为:Na2CO3+CO2+H2O=2NaHCO3.
17.早期化学家为了认识空气的本质,将一些物质放在密闭的容器中进行实验,结果发现:每次都有约$\frac{1}{5}$的空气不知去向.当时化学家把这$\frac{1}{5}$的空气称为“有用空气”这种“有用空气”是指( )
| A. | 氮气 | B. | 二氧化碳 | C. | 氧气 | D. | 稀有气体 |
1.将M克Zn加入到一定质量的AgNO3和Cu(NO3)2的混合溶液中,充分反应后过滤,将滤渣洗涤、干燥后再称量,得到的固体质量仍为M克.据此,下列说法不正确的是( )
| A. | 反应后的滤液中有三种溶质 | |
| B. | 取反应后的滤液观察,滤液可能呈蓝色 | |
| C. | 取滤渣滴加稀硫酸,可能有气泡产生 | |
| D. | 滤渣中的物质至少有两种 |
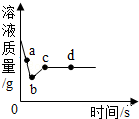 向一定质理AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间变化的情况如图所示.
向一定质理AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间变化的情况如图所示.
 ,它属于非金属(填“金属”与“非金属”)元素;化学反应中该原子比较容易得到(填“得到”或“失去”)电子变成离子,该离子符号是S2-.
,它属于非金属(填“金属”与“非金属”)元素;化学反应中该原子比较容易得到(填“得到”或“失去”)电子变成离子,该离子符号是S2-.