题目内容
在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种。同学们为了确定该粉末的成分,进行如下探究。请你参与他们的探究并回答问题。
(1)【提出问题】假设l:红色粉末是铜粉;假设2:红色粉末是氧化铁粉;
假设3:红色粉末是_________________
(2)【设计实验方案】 同学们对实验作了如下设想和分析:取少量红色粉末放入硬质玻璃管中,通入一氧化碳片刻后加热至充分反应(实验装置如右图所示)。
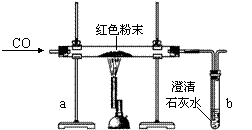
若假设1成立,在实验中可看到的现象是
若假设2成立,在实验中可看到的现象是 ;
若假设3成立,在实验中可看到的现象是 ;
(3)【进行实验】通过实验及分析,确认假设3成立。
(4)【反思与评价】
①实验过程中,硬质玻璃管内发生反应的化学方程式是__________________
②实验时通入一氧化碳片刻后再加热的原因是____________________
③从环保角度看,上面的实验装置有不足之处,请你对该装置进行改进,具体措施是__________________________________________
(5)【拓展】为了进一步探究铁和铜的金属活动性强弱,请根据实验室现有的仪器和药品条件(如下所列),通过填写下表,完成对实验方案的构思。
【实验仪器】试管、胶头滴管、镊子
【实验药品】铁钉、铜片、稀硫酸、硫酸锌溶液、硫酸亚铁溶液、硫酸铜溶液
| 所选药品 | 有关化学方程式 |
(1)铜粉和氧化铁粉的混合物;
(2)
| 红色粉末不变色,石灰水不变浑浊 | 假设l |
| 红色粉末全部变为黑色,石灰水变浑浊 | 假设2 |
| 红色粉末部分变为黑色,石灰水变浑浊 | 假设3 |
(4) ①3CO+Fe2O3![]() 2Fe+3CO2
2Fe+3CO2
②防止加热一氧化碳和空气的混合气体时发生爆炸
③在b处用酒精灯点燃 [ 或用塑料袋(气球)收集 ]
(5)(只需写出1个方案,合理均给分)
| 方案 | 所选药品 | 有关化学方程式 |
| 1 | 铁钉、铜片、稀硫酸 | Fe+H2SO4 == FeSO4+H2↑ |
| (或2) | 或(铁钉、硫酸铜溶液) | 或( Fe+CuSO4 == FeSO4+Cu ) |

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案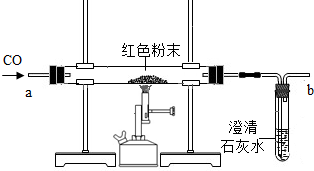 在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.
在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.(1)【提出问题】假设l:红色粉末是铜粉;假设2:红色粉末是氧化铁粉;
假设3:红色粉末是
(2)【设计实验方案】同学们对实验作了如下设想和分析:取少量红色粉末放入硬质玻璃管中,通入一氧化碳片刻后加热至充分反应(实验装置如图所示).
请你完成下表:
| 实验中可能出现的现象 | 结论 |
| 假设1成立 | |
| 假设2成立 | |
| 假设3成立 |
(4)【反思与评价】
①实验过程中,硬质玻璃管内发生反应的化学方程式是
②实验时通入一氧化碳片刻后再加热的原因是
③从环保角度看,上面的实验装置有不足之处,请你对该装置进行改进,具体措施
是
(5)【拓展】为了进一步探究铁和铜的金属活动性强弱,请根据实验室现有的仪器和药品条件(如下所列),通过填写下表,完成对实验方案的构思.
[实验仪器]试管、胶头滴管、镊子
[实验药品]铁钉、铜片、稀硫酸、硫酸锌溶液、硫酸亚铁溶液、硫酸铜溶液
| 所选药品 | 有关化学方程式 |
 在实验探究课上,老师给了同学们一包红色粉末,该粉末是铜粉和氧化铁(Fe2O3)粉末中的一种或两种.
在实验探究课上,老师给了同学们一包红色粉末,该粉末是铜粉和氧化铁(Fe2O3)粉末中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究活动并回答问题.
(1)[提出问题]
假设1:红色粉末是铜粉;
假设2:红色粉末是氧化铁粉;
假设3:红色粉末是
(2)[设计实验方案]同学们为了验证上述假设,
设计了如上图所示实验装置,并对实验结果作了如下设想和分析:取少量红色粉末放人硬质玻璃管中,通入一氧化碳,片刻后加热至充分反应.
请你完成下表:
| 实验中可能出现的现象 | 结论 |
| 假设1成立 | |
| 假设2成立 | |
| 假设3成立 |
(4)[反思与评价]
①实验过程中,硬质玻璃管内发生反应的化学方程式是:
②实验时,先通入一氧化碳片刻后再加热的原因是:
③从环保角度看,上面的实验装置有不足之处,请你对该装置进行改进,具体措施是

