题目内容
19.2015年3月28日是本年度的“地球一小时”(Earth Hour)活动日,主题为“能见蔚蓝”,旨在呼吁每一位公民从自身开始,采取实际行动,应对当前中国最急迫、最受关注的环境议题--雾霾.作为一名中学生,你认为下列做法不应该提倡的是( )| A. | 拒绝使用一次性木筷,提倡反复使用塑料袋 | |
| B. | 将废纸、汽水瓶等收集起来,进行统一焚烧 | |
| C. | 纸张提倡双面使用,用电子贺卡代替纸制贺卡 | |
| D. | 选择自行车和公交车作为出行工具 |
分析 A、拒绝一次性使用一次性木筷,不使用一次性塑料袋,可节约能源保护环境;
B、将废纸、汽水瓶等收集起来,一次性焚烧,会污染空气;
C、节约用纸,用电子贺卡代替纸制贺卡,可以节约能源保护环境;
D、选择自行车和公交车作为出行工具,可以节约能源保护环境.
解答 解:A、不使用一次性塑料袋,可节约能源保护环境;
B、将 废纸、汽水瓶等收集起来,一次性焚烧,会污染空气;
C、节约用纸,用电子贺卡代替纸制贺卡,可以节约能源保护环境;
D、选择自行车和公交车作为出行工具,可以节约能源保护环境.
故选B.
点评 环保问题已经引起了全球的重视,关于“三废”的处理问题,是中考的热点问题,化学上提倡绿色化学工艺,要从源头减少污染.

练习册系列答案
 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案
相关题目
10.能源和环境是人类生存的基本条件,下列叙述错误的是( )
| A. | 氢气是清洁高能燃料 | B. | 石油是一种不可再生能源 | ||
| C. | 过量排放CO2会形成酸雨 | D. | 淘汰落后产能可减少环境污染 |
7.通过如图所示实验可以得出的结论中不合理的是( )
| A. |  实验中黄铜片能在铜片上刻画出痕迹并不能说明黄铜的密度比铜片大 | |
| B. |  实验既可以说明分子在不停地运动着,又可以说明氨水显碱性 | |
| C. |  实验既可以说明二氧化碳易溶于水,又可以说明二氧化碳具有酸性 | |
| D. |  实验既可以说明一氧化碳具有还原性,又可以说明一氧化碳具有可燃性 |
14.今年全国人大和政协会议使用了一种含碳酸钙的“石头纸”,为测定其中碳酸钙的含量,课外活动小组的同学称取50g碎纸样品.分别在5只烧杯中进行了实验,实验数据见下表(假设纸张中其他成分既不溶于水,也不与酸反应):
(1)表中X的值为2.64;
(2)求样品中碳酸钙的质量分数;(完成计算过程,下同)
(3)烧杯④中物质充分反应后所得溶液的质量分数.(计算结果精确到0.1%)
| 烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
| 加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
| 加入稀盐酸的质量/g | 15 | 30 | 45 | 60 | 75 |
| 充分反应后生成气体的质量/g | 0.88 | 1.76 | X | 3.52 | 3.52 |
(2)求样品中碳酸钙的质量分数;(完成计算过程,下同)
(3)烧杯④中物质充分反应后所得溶液的质量分数.(计算结果精确到0.1%)
4.关于下列化学用语的说法正确的是( )
①H2 ②Ca2+ ③NO2 ④ ⑤
⑤
①H2 ②Ca2+ ③NO2 ④
 ⑤
⑤
| A. | ①可表示两个氢原子 | B. | ③中氮元素的化合价为+4 | ||
| C. | ②和⑤均表示阳离子 | D. | ④和⑤表示的微粒化学性质相同 |
11.一种名为“污渍爆炸盐”的洗涤产品能高效去除衣物上的顽固污渍,是当前使用最为广泛的洗涤助剂之一.某校化学兴趣小组的同学在老师的指导下对该产品开展了以下探究活动.
【查阅资料】
“污渍爆炸盐”的主要成分是过碳酸钠(Na2CO4,相对分子质量为122),它是一种白色粉末,易溶于水,且能与水反应,生成一种碳酸盐和一种强氧化性的物质.
【实验探究一】过碳酸钠的性质
为探究过碳酸钠的性质,同学们设计了以下实验,请按要求完成表格内容:
【实验探究二】过碳酸钠的含量测定
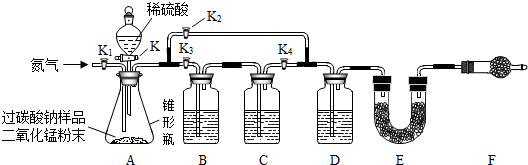
同学们经讨论设计了如图所示的实验装置.图中装置B盛装氢氧化钠溶液,C盛装澄清石灰水,D盛装浓硫酸,E、F均装入干燥的碱石灰(主要成分:氧化钙和氢氧化钠的固体混合物;可吸收二氧化碳和水蒸气).
【实验讨论】
(1)①称量装置E的质量;②组装好装置,检查气密性,装入药品;③关闭活塞K,打开活塞K1,通入氮气;④关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气;⑤依次关闭活塞K1、K3、K4,打开活塞K K2、,直到反应不再进行;⑥再次称量装置E的质量.
以上实验步骤的正确顺序是D;
A.①②③④⑤⑥B.②①④⑤③⑥C.①②④⑤③⑥D.②④①⑤③⑥
(2)关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气排出装置中原有的空气,此时装置B的作用是除去原有空气中的二氧化碳,防止空气中的二氧化碳进入E装置;
(3)反应完全后关闭活塞K,打开活塞K1,通入氮气的目的是将装置中残留的二氧化碳排出,被E装置充分吸收;
(4)同学们称取6.63g含碳酸钠杂质的过碳酸钠样品(不含其他杂质)进行实验,根据实验后E装置增重2.42g,求该样品中过碳酸钠的含量(写出计算过程,结果保留小数点后一位).
(5)装置F的作用是防止空气中的二氧化碳和水蒸气进入E装置,干扰实验,若不连接装置F,测定的过碳酸钠含量会偏低(填“偏高”或“偏低”).
【查阅资料】
“污渍爆炸盐”的主要成分是过碳酸钠(Na2CO4,相对分子质量为122),它是一种白色粉末,易溶于水,且能与水反应,生成一种碳酸盐和一种强氧化性的物质.
【实验探究一】过碳酸钠的性质
为探究过碳酸钠的性质,同学们设计了以下实验,请按要求完成表格内容:
| 序号 | 实验步骤 | 实验现象 | 实验分步结论(或解释) |
| ① | 向盛有过碳酸钠固体的试管中加入适量水 | 固体溶解 | 过碳酸钠易溶于水, 能与水发生反应. |
| ② | 向序号①的所得溶液中加入适量的二氧化锰粉末 | 有大量气泡 产生 | |
| ③ | 将带火星的木条置于试管口 | 木条复燃 | 序号②试管中产生的气体是O2; 过碳酸钠溶于水能生成过氧化氢. |
| ④ | 取序号③试管中的上层清液加入氯化钙溶液 | 产生白色 沉淀 | 反应的化学方程式Na2CO3+CaCl2═CaCO3↓+2NaCl. |
| 小结 | 过碳酸钠与水反应的化学方程式是Na2CO4+H2O═Na2CO3+H2O2. | ||
同学们经讨论设计了如图所示的实验装置.图中装置B盛装氢氧化钠溶液,C盛装澄清石灰水,D盛装浓硫酸,E、F均装入干燥的碱石灰(主要成分:氧化钙和氢氧化钠的固体混合物;可吸收二氧化碳和水蒸气).

【实验讨论】
(1)①称量装置E的质量;②组装好装置,检查气密性,装入药品;③关闭活塞K,打开活塞K1,通入氮气;④关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气;⑤依次关闭活塞K1、K3、K4,打开活塞K K2、,直到反应不再进行;⑥再次称量装置E的质量.
以上实验步骤的正确顺序是D;
A.①②③④⑤⑥B.②①④⑤③⑥C.①②④⑤③⑥D.②④①⑤③⑥
(2)关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气排出装置中原有的空气,此时装置B的作用是除去原有空气中的二氧化碳,防止空气中的二氧化碳进入E装置;
(3)反应完全后关闭活塞K,打开活塞K1,通入氮气的目的是将装置中残留的二氧化碳排出,被E装置充分吸收;
(4)同学们称取6.63g含碳酸钠杂质的过碳酸钠样品(不含其他杂质)进行实验,根据实验后E装置增重2.42g,求该样品中过碳酸钠的含量(写出计算过程,结果保留小数点后一位).
(5)装置F的作用是防止空气中的二氧化碳和水蒸气进入E装置,干扰实验,若不连接装置F,测定的过碳酸钠含量会偏低(填“偏高”或“偏低”).