题目内容
12.有一固体混合物,可能由Na2CO3、FeCl3、BaCl2、Na2SO4、NaCl中的一种或几种混合而成,实验过程及实验现象如图所示.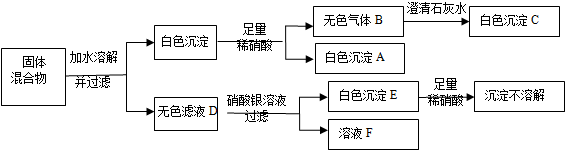
(1)请写出白色沉淀A的化学式为BaSO4,白色沉淀E的化学式AgCl.
(2)原固体混合物中一定含有的物质是Na2CO3、BaCl2、Na2SO4,一定没有的物质是FeCl3.
(3)无色气体B与澄清石灰水反应的化学方程式是CO2+Ca(OH)2=CaCO3↓+H2O.
分析 依据混合物溶于水后会生成沉淀,且该沉淀部分溶于稀硝酸且能生成使澄清石灰水变浑浊的二氧化碳气体,可知该沉淀是氯化钡和碳酸钠、硫酸钠反应产生的碳酸钡沉淀和硫酸钡沉淀,所以固体中一定含有氯化钡和碳酸钠、碳酸钠;滤液是无色的,因此一定不含有氯化铁;向滤液加入硝酸银和稀硝酸后还有沉淀出现,则说明该滤液中含有氯离子,而氯化钡中含有氯离子,所以氯化钠是否含有无法确定,据此分析解答即可.
解答 解:依据混合物溶于水后会生成沉淀,且该沉淀部分溶于稀硝酸且能生成使澄清石灰水变浑浊的二氧化碳气体,可知该沉淀是氯化钡和碳酸钠、硫酸钠反应产生的碳酸钡沉淀和硫酸钡沉淀,所以固体中一定含有氯化钡和碳酸钠、碳酸钠;滤液是无色的,因此一定不含有氯化铁;向滤液加入硝酸银和稀硝酸后还有沉淀出现,则说明该滤液中含有氯离子,而氯化钡中含有氯离子,所以氯化钠是否含有无法确定;
(1)由分析知A是碳酸钡;E是氯化银;故填:BaSO4 AgCl;
(2)由分析知白色固体中一定含有的物质是碳酸钠、氯化钡和硫酸钠;一定不含有氯化铁;故答案为:Na2CO3、BaCl2、Na2SO4;FeCl3;
(3)无色气体B与澄清石灰水反应是二氧化碳和氢氧化钙反应产生碳酸钙沉淀和水,故反应的方程式为:CO2+Ca(OH)2=CaCO3↓+H2O.
点评 本题为推断题对于推断题的解法,要根据题给条件和物质的化学特性找准突破口,然后顺藤摸瓜判断原混合物的组成,然后进行解答.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
3. 向一定量某固体中逐滴加入某溶液至过量,x轴表示加入溶液的质量.下列选项中y轴表示的含义与所给图象变化趋势一致的是( )
向一定量某固体中逐滴加入某溶液至过量,x轴表示加入溶液的质量.下列选项中y轴表示的含义与所给图象变化趋势一致的是( )
 向一定量某固体中逐滴加入某溶液至过量,x轴表示加入溶液的质量.下列选项中y轴表示的含义与所给图象变化趋势一致的是( )
向一定量某固体中逐滴加入某溶液至过量,x轴表示加入溶液的质量.下列选项中y轴表示的含义与所给图象变化趋势一致的是( )| 选项 | 固 体 | 溶 液 | y 轴 含 义 |
| A | 二氧化锰 | 过氧化氢溶液 | 水的质量 |
| B | 大理石(杂质不反应) | 稀盐酸 | 固体中杂质的质量分数 |
| C | 铁粉与铜粉混合粉末 | 硫酸铜溶液 | 所得溶液中硫酸铜的质量 |
| D | 氯化钠与碳酸钠混合粉末 | 稀硫酸 | 二氧化碳的体积 |
| A. | A | B. | B | C. | C | D. | D |
20.如图为某反应的微观示意图,则下列说法不正确的是( )
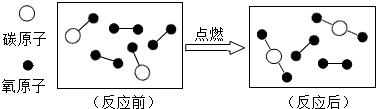

| A. | 反应后的物质是混合物 | |
| B. | 参加反应的CO、O2、CO2的分子个数比为2:3:2 | |
| C. | 该反应属于化合反应 | |
| D. | 反应前后原子的种类、数目都没有发生改变 |
17.等离子空气净化器在工作时会产生臭氧(O3),臭氧是一种公认的高效空气杀菌剂,但达到一定浓度时对人体也有害,不仅有臭味,也可能致癌.下列说法正确的是( )
| A. | 臭氧转变为氧气是物理变化 | |
| B. | 臭氧能吸收紫外线,保护地球上的生物免受紫外线的伤害 | |
| C. | 臭氧能杀菌,所以空气中臭氧浓度越高越好 | |
| D. | 等质量的臭氧和氧气含有相同分子数 |
2.以石灰石为原料,可以生产生石灰,生石灰可做干燥剂,某科学兴趣小组的同学对食品厂某批次包装完整、粉状的生石灰成分进行质量检测.

【提出问题】该批次的生石灰成分及含量是否与标签相符?(标签如图1所示)
【猜想与假设】固体成分为:
A:全部是碳酸钙和杂质 B:既有碳酸钙,也有氧化钙和杂质 C:氧化钙
【设计并完成实验】
【实验结论】该兴趣小组同学得出的结论是:样品中既有碳酸钙,也有氧化钙和杂质
【定量测定】称取10克该批次的生石灰样品(图2),置于锥形瓶中,向其中缓慢加稀盐酸,直至无气泡产生,电子天平读数减小0.88克,将锥形瓶中残留物进行过滤、洗涤、干燥,得到固体质量为0.2克.通过计算求出生石灰的含量.

【提出问题】该批次的生石灰成分及含量是否与标签相符?(标签如图1所示)
【猜想与假设】固体成分为:
A:全部是碳酸钙和杂质 B:既有碳酸钙,也有氧化钙和杂质 C:氧化钙
【设计并完成实验】
| 实验操作 | 实验现象 | 实验结论 |
| 第一步操作:取少量固体于试管中,加适量水振荡后静置,再滴几滴无色酚酞试液 | 溶液变红 | 说明固体成分中一定含有①氧化钙 |
| 第二步操作:再取少量固体于另一试管中滴加过量稀盐酸 | 有气泡生成 | 说明固体成分中一定含有②碳酸钙 |
【定量测定】称取10克该批次的生石灰样品(图2),置于锥形瓶中,向其中缓慢加稀盐酸,直至无气泡产生,电子天平读数减小0.88克,将锥形瓶中残留物进行过滤、洗涤、干燥,得到固体质量为0.2克.通过计算求出生石灰的含量.
 下列选项中,各概念之间能构成图中包含关系的是( )
下列选项中,各概念之间能构成图中包含关系的是( )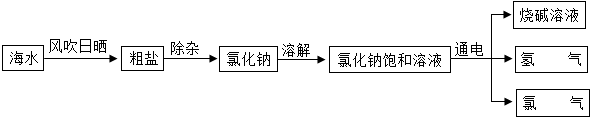
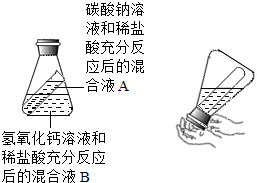 甲、乙两同学在学完酸的化学性质后,分别做了如下两个实验A、B.然后,他们又将各自的混合液混合.(先将锥形瓶慢慢倒转,使试管中的A液体流入锥形瓶B液体中)
甲、乙两同学在学完酸的化学性质后,分别做了如下两个实验A、B.然后,他们又将各自的混合液混合.(先将锥形瓶慢慢倒转,使试管中的A液体流入锥形瓶B液体中) 世界环保联盟建设全面禁止用氯气(常温下是一种黄绿色有毒气体)对饮用水消毒,推广使用安全、高效杀菌消毒剂ClO2.ClO2是一种黄绿色,有刺激性气味的气体,冷却至11.0℃以下时变成红色液体,易溶于水,见光易分解,易与碱反应,杀菌、漂白能力均优于氯气.
世界环保联盟建设全面禁止用氯气(常温下是一种黄绿色有毒气体)对饮用水消毒,推广使用安全、高效杀菌消毒剂ClO2.ClO2是一种黄绿色,有刺激性气味的气体,冷却至11.0℃以下时变成红色液体,易溶于水,见光易分解,易与碱反应,杀菌、漂白能力均优于氯气.