题目内容
7.海洋是一个巨大的资源宝库,我们可以从海水中提取氯化钠,并以氯化钠和水为原料制得氢氧化钠、氢气和氯气(Cl2).其制取的主要工艺流程如图所示: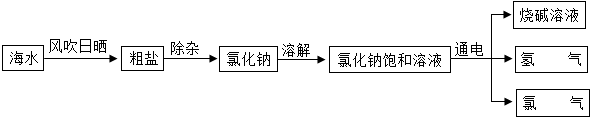
(1)利用风吹日晒从海水中提取粗盐,该过程主要发生物理变化(填“物理”或“化学”).
(2)氯化钠饱和溶液在通电条件下发生反应的化学方程式是:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
分析 根据已有的知识进行分析解答,风吹日晒的过程中没有产生新的物质,是物理变化;氯化钠的饱和溶液通电能生成氢氧化钠、氢气和氯气,据此解答.
解答 解:(1)风吹日晒从海水中提取粗盐,该过程没有产生新的物质,发生的是物理变化,故填:物理;
(2)氯化钠饱和溶液在通电条件下能生成氢氧化钠、氢气和氯气,反应的化学方程式为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.故填:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
点评 本题考查的是海洋资源的应用的知识,完成此题,可以依据已有的知识进行.书写反应的化学方程式要注意配平.

练习册系列答案
相关题目
18.实验操作有误或不规范,很可能造成实验失败或酿成事故,下列图示实验操作正确的是( )
| A. |  稀释浓硫酸 | B. |  测液体的pH值 | C. |  称取10.5克NaCl | D. |  熄灭酒精灯 |
15.下列选项中属于纯净物的是( )
| A. | 水 | B. | 空气 | C. | 食盐水 | D. | 石灰水 |
16.小明欲测量一石灰石中CaCO3的质量分数,将100g盐酸平均分5次加入到30g石灰石样品中(已知杂质不与盐酸反应也不溶于水,CaCO3与盐酸反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑),得到如下数据.
(1)第2次加入盐酸后,a为20克.
(2)石灰石样品中碳酸钙的质量是20克.
(3)第4次实验后生成的CaCl2溶液的溶质质量分数是多少?(列式计算,结果精确到0.1%)
| 次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 剩余固体的质量/g | 25 | a | 15 | 10 | 10 |
(2)石灰石样品中碳酸钙的质量是20克.
(3)第4次实验后生成的CaCl2溶液的溶质质量分数是多少?(列式计算,结果精确到0.1%)
17.若用实验证明CuSO4溶液显蓝色不是由SO42-离子造成的.下列实验无意义的是( )
| A. | 观察K2SO4溶液的颜色 | |
| B. | 加水稀释后CuSO4溶液颜色变浅 | |
| C. | 向CuSO4溶液滴加适量的NaOH溶液,振荡后静置,溶液颜色消失 | |
| D. | 向CuSO4溶液滴加适量的BaCl2溶液,振荡后静置,溶液颜色未消失 |
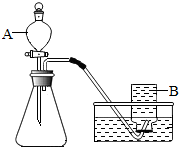 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.