题目内容
17.河北迁安以钢铁为主要产业,某化学兴趣小组用如图a所示装置探究炼铁的原理.请回答有关问题:
(1)实验开始时,应先加热再通CO(选填“先加热再通CO”或“先通CO再加热”),目的是排净玻璃管中的空气,防止一氧化碳与空气混合发生爆炸.
(2)试验结束后,应先停止加热(选填“先停止加热”或“先停止通CO”),目的是防止再次被氧化灼热的铁.
(3)玻璃管A中出现的现象为红色粉末变黑;反应方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(4)高炉炼铁中的焦炭也具有还原性,但实际上炼铁主要利用了CO的性质,其原因是一氧化碳具有流动性,能与铁矿石充分接触.焦炭的作用提供热量、产生一氧化碳.
(5)在工业生产中,企业要测定矿石的品味(即主要成分的质量分数),该兴趣小组利用如图b装置,设计了实验方案(装置气密性良好;赤铁矿粉中杂质不参与反应;假设赤铁矿粉样品中的Fe2O3完全反应);他们通过测定反应前后玻璃管中固体质量的变化等数据,再通过计算可以得出赤铁矿粉样品中Fe2O3的质量分数.
(6)为防止实验中尾气对大气的污染,请写出处理尾气的一种方法在装置的末端加一个燃着的酒精灯.
分析 (1)根据一氧化碳易可燃,容易发生爆炸考虑;
(2)根据灼热的铁能与氧气反应分析回答;
(3)根据在高温条件下一氧化碳与氧化铁的反应分析回答;
(4)根据一氧化碳是气体能与铁矿石成分接触和碳的性质分析回答;
(5)根据在高温条件下一氧化碳与氧化铁的反应分析回答;
(6)根据尾气中含有一氧化碳有毒能污染空气分析回答.
解答 解:(1)因为一氧化碳具有可燃性,能和氧气混合在点燃的条件下会发生爆炸,实验开始时,应先加热再通CO,目的是排净玻璃管中的空气,防止一氧化碳与空气混合发生爆炸.
(2)试验结束后,应先停止加热,目的是防止再次被氧化灼热的铁.
(3)红色的氧化铁和一氧化碳在高温条件下反应能生成铁和二氧化碳,所以玻璃管A中出现的现象是红色粉末变黑,其化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(4)高炉炼铁中的焦炭也具有还原性,但实际上炼铁主要利用了CO的性质,其原因是一氧化碳具有流动性,能与铁矿石充分接触.由于谈成分燃烧生成了二氧化碳,放出了大量的热,二氧化碳能与碳反应生成了一氧化碳,所以焦炭的作用提供热量、产生一氧化碳.
(5)在工业生产中,企业要测定矿石的品味(即主要成分的质量分数),该兴趣小组利用如图b装置,设计了实验方案(装置气密性良好;赤铁矿粉中杂质不参与反应;假设赤铁矿粉样品中的Fe2O3完全反应);他们通过测定反应前后玻璃管中固体质量的变化等数据,再通过计算可以得出赤铁矿粉样品中Fe2O3的质量分数.
(6)为防止实验中尾气对大气的污染,处理尾气的一种方法是:在装置的末端加一个燃着的酒精灯.
故答案为:
(1)先通CO再加热;排净玻璃管中的空气,防止一氧化碳与空气混合发生爆炸;
(2)先停止加热,防止再次被氧化灼热的铁
(3)红色粉末变黑;3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(4)一氧化碳具有流动性,能与铁矿石充分接触,提供热量、产生一氧化碳;
(5)反应前后玻璃管中固体质量的变化;
(6)在装置的末端加一个燃着的酒精灯.
点评 本题主要考查一氧化碳与氧化铁反应实验装置、实验现象、一氧化碳的化学性质和污染及能源的再利用,难度稍大.

| A. | 硫 | B. | 水 | C. | 汞 | D. | 氯化钠 |
| A. | 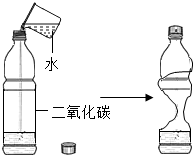 旋紧瓶盖振荡, 旋紧瓶盖振荡,塑料瓶变瘪 | |
| B. | 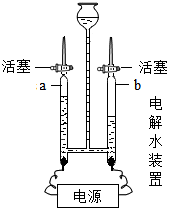 用燃着的木条 用燃着的木条a管尖嘴口检验 产生的气体,木条 燃烧更旺 | |
| C. |  黄铜片在纯铜片 黄铜片在纯铜片上刻画时留下痕迹 | |
| D. | 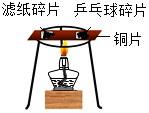 滤纸碎片先燃烧,乒乓球碎片后燃烧 滤纸碎片先燃烧,乒乓球碎片后燃烧 |