题目内容
5.下列叙述中,不正确的是( )| A. | 硬水易生水垢 | |
| B. | 地球上可利用的淡水资源是有限的 | |
| C. | 软水与肥皂作用不易起泡沫 | |
| D. | 生活污水的任意排放会造成水体的污染 |
分析 本题主要考查学生对硬水和软水的认识,还涉及水资源的保护,要用所学知识对每一项加以分析,硬水是指含有较多的可溶性的钙、镁化合物的水,当加入肥皂水后,会出现较多的浮渣,煮沸后硬水变成软水,钙、镁化合物将变成水垢沉淀下来.地球上可供人类直接利用的淡水资源不足总水量的1%,因此我们要爱护水资源,防止水的污染.
解答 解:A、硬水易生水垢,因为硬水中含有较多的可溶性的钙、镁化合物,当煮沸后硬水变成软水,钙、镁化合物将变成水垢沉淀下来,故A正确;
B、地球上水很多,但绝大部分是海水,淡水较少,而供人类直接利用的淡水资源不足总水量的1%,故B正确;
C、鉴别硬水和软水的方法:加入肥皂水,泡沫多浮渣少的是软水,泡沫少浮渣多的是硬水,故C错误;
D、生活污水随意排放,生活污水尽管没有工业污水中有害物质多,但生活污水好有较多的洗涤剂残留物和富营养物质(如氮磷),对水体的污染也不能忽视,故D正确.
故选C.
点评 本题较为简单,根据书本所学知识即可解答,但要有爱护水资源的环保意识.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
13.某化学兴趣小组围绕“酸碱中和反应”,在老师引导下开展探究活动.
探究Ⅰ:证明氢氧化钠溶液与稀盐酸确实能发生反应.
【方案1】测定稀盐酸与NaOH溶液混合前后的pH.
测定某NaOH溶液的pH,pH大于7.将一定量的稀盐酸加入该NaOH溶液中,混合均匀后测定其pH,发现pH减小了,但仍然大于7,小组中有的同学认为根据这个测定结果可以认为稀盐酸与NaOH溶液发生了反应,你认为他们的结论是否正确:不正确,理由氢氧化钠溶液中加水稀释pH也会减小.经过讨论后,他们向溶液中又加入一定量的稀盐酸,混合均匀后测定其pH,pH 小于7.
结论:稀盐酸与氢氧化钠溶液发生了化学反应,并且稀盐酸过量.
【方案2】借助于无色酚酞试液.
【药品仪器】如图1
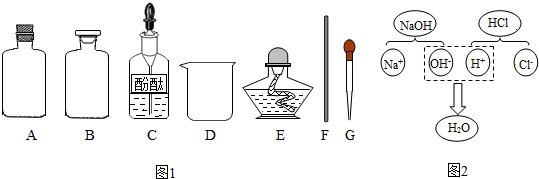
①取A(选填“A”或“B”)中试剂加入至D中,滴加2滴酚酞试液,溶液呈红色;
②用胶头滴管向①中溶液滴加稀盐酸,红色消失;
③用F蘸取②中溶液,在酒精灯上灼烧,有白色固体产生.
【思考拓展】
(1)如不使用酸碱指示剂,进一步确认步骤③中的白色固体不是氢氧化钠的方法是:取少量水将其溶解加入CuSO4溶液,无蓝色沉淀.
(2)探究步骤②中无色溶液中稀盐酸是否过量.
根据上述反应过程中溶液变成无色,不能确定稀盐酸是否过量,兴趣小组同学又分别选取了AgNO3溶液、紫色石蕊试液、Na2CO3粉末设计实验方案,请你分析并判断:
方案③中反应的化学方程式6HCl+Fe2O3═Fe2Cl3+3H2O.上述设计方案中,不正确的是①(填“①”、“②”或“③”),错误的原因是反应生成的NaCl也能与AgNO3反应生成白色沉淀,不能证明溶液中含有盐酸.
请你再设计一个与上述实验不同原理的方案以确定稀盐酸是否过量,你选用的试剂是Na2CO3溶液或锌等.
(3)不是所有的碱与盐酸反应都无明显现象,例如Cu(OH)2(填一种碱)与盐酸反应就有明显的实验现象.
探究Ⅱ:从微观的角度认识物质及其变化的本质.图2表示氢氧化钠溶液与盐酸反应的微观过程,该反应的本质是氢离子和氢氧根离子;结合生成水.请写出一个与上述反应本质相同的化学方程式:2NaOH+H2SO4=Na2SO4+2H2O.
探究Ⅰ:证明氢氧化钠溶液与稀盐酸确实能发生反应.
【方案1】测定稀盐酸与NaOH溶液混合前后的pH.
测定某NaOH溶液的pH,pH大于7.将一定量的稀盐酸加入该NaOH溶液中,混合均匀后测定其pH,发现pH减小了,但仍然大于7,小组中有的同学认为根据这个测定结果可以认为稀盐酸与NaOH溶液发生了反应,你认为他们的结论是否正确:不正确,理由氢氧化钠溶液中加水稀释pH也会减小.经过讨论后,他们向溶液中又加入一定量的稀盐酸,混合均匀后测定其pH,pH 小于7.
结论:稀盐酸与氢氧化钠溶液发生了化学反应,并且稀盐酸过量.
【方案2】借助于无色酚酞试液.
【药品仪器】如图1

①取A(选填“A”或“B”)中试剂加入至D中,滴加2滴酚酞试液,溶液呈红色;
②用胶头滴管向①中溶液滴加稀盐酸,红色消失;
③用F蘸取②中溶液,在酒精灯上灼烧,有白色固体产生.
【思考拓展】
(1)如不使用酸碱指示剂,进一步确认步骤③中的白色固体不是氢氧化钠的方法是:取少量水将其溶解加入CuSO4溶液,无蓝色沉淀.
(2)探究步骤②中无色溶液中稀盐酸是否过量.
根据上述反应过程中溶液变成无色,不能确定稀盐酸是否过量,兴趣小组同学又分别选取了AgNO3溶液、紫色石蕊试液、Na2CO3粉末设计实验方案,请你分析并判断:
| 实验方案 | 实验步骤 | 现 象 | 结 论 |
| ① | 取样,加入适量的AgNO3溶液 | 出现白色沉淀 | 稀盐酸过量 |
| ② | 取样,加入几滴紫色石蕊试液 | 溶液变红 | 稀盐酸过量 |
| ③ | 取样,加入铁锈粉末 | 红棕色粉末逐渐减少,溶液变成黄色 | 稀盐酸过量 |
请你再设计一个与上述实验不同原理的方案以确定稀盐酸是否过量,你选用的试剂是Na2CO3溶液或锌等.
(3)不是所有的碱与盐酸反应都无明显现象,例如Cu(OH)2(填一种碱)与盐酸反应就有明显的实验现象.
探究Ⅱ:从微观的角度认识物质及其变化的本质.图2表示氢氧化钠溶液与盐酸反应的微观过程,该反应的本质是氢离子和氢氧根离子;结合生成水.请写出一个与上述反应本质相同的化学方程式:2NaOH+H2SO4=Na2SO4+2H2O.
10.具有保存价值的档案、账本应用碳素墨水书写,这是因为( )
| A. | 碳具有氧化性 | B. | 碳具有还原性 | ||
| C. | 碳能与纸发生反应 | D. | 碳在常温下性质稳定 |
17.下列实验操作正确的是( )
| A. |  熄灭酒精灯 | B. |  量筒的读数 | ||
| C. |  加热液体 | D. |  用高锰酸钾制氧气 |
14.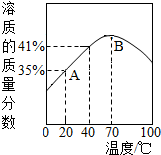 ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示.下列说法正确的是( )
ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示.下列说法正确的是( )
 ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示.下列说法正确的是( )
ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示.下列说法正确的是( )| A. | ZnSO4饱和溶液的溶质质量分数随温度升高而增大 | |
| B. | 点A对应的ZnSO4溶液是不饱和溶液 | |
| C. | 点B对应的ZnSO4溶液升温或降温均能达到饱和 | |
| D. | 40℃时,ZnSO4的溶解度为41g |

