题目内容
20.汽车是现代生活中不可缺少的代步工具.请回答下列问题:汽车电路中的导线大都是铜制的,这是利用了金属铜的延展性和导电性,作为化学电源,氢氧燃料电池已经被应用,氢氧燃料电池用作汽车的驱动电源行驶时的能量转化是化学能→电能(用“→”表示转化).铜在潮湿的环境中因氧化与空气中的成分反应而缓慢生成铜绿Cu2(OH)2CO3,写出该化学反应方程式2Cu+O2+H2O+CO2═Cu2(OH)2CO3,反应前后铜元素的化合价变化为0→+2.下列汽车配件及用品中,属于有机合成材料的是c(填序号,下同),该合成材料的优点耐磨、价廉.(写二条)
分析 根据金属具有优良的导电性和延展性,氢氧燃料电池用作汽车的驱动电源行驶时,是将化学能转化为电能,铜、氧气、水和二氧化碳反应生成碱式碳酸铜,反应前铜是单质,显0价,反应后铜显示+2价,材料分为金属材料、硅酸盐材料、有机高分子材料(即合成有机高分子材料、天然有机高分子材料)进行分析.
解答 解:汽车电路中的导线大都是铜制的,这是利用了金属铜的延展性和导电性,作为化学电源,氢氧燃料电池已经被应用,氢氧燃料电池用作汽车的驱动电源行驶时的能量转化是:化学能→电能,铜、氧气、水和二氧化碳反应生成碱式碳酸铜,化学方程式为:2Cu+O2+H2O+CO2═Cu2(OH)2CO3,反应前铜是单质,显0价,反应后铜显示+2价,所以反应前后铜元素的化合价变化为0→+2,a属于金属材料,b属于硅酸盐材料,c属于合成有机高分子材料(简称合成材料),d属于天然有机高分子材料;故选:c,该合成材料的优点是耐磨、价廉.
故答案为:导电性,化学能→电能,2Cu+O2+H2O+CO2═Cu2(OH)2CO3,0→+2,c,耐磨、价廉.
点评 本题从金属的利用,材料的鉴别,锈蚀及保存等方面全面考查了金属的性质,是一道不错的试题.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
10.下列不属于化学变化的是( )
| A. | 葡萄酿酒 | B. | 煤的干馏 | ||
| C. | 熟石灰改良酸性土壤 | D. | 石油的分馏 |
11.有一种石灰石样品的成分是CaCO3和SiO2(已知SiO2既不溶于水也不与盐酸反应).现将10g石灰石样品放入烧杯中,再将100g稀盐酸分4次加入烧杯中,每次均充分反应.实验数据记录如下:
求:(1)上述表格中M的值为2
(2)该石灰石样品中碳酸钙的质量分数.
(3)该稀盐酸的溶质质量分数.
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
| 充分反应后剩余固体质量/g | 7 | 4 | 2 | M |
(2)该石灰石样品中碳酸钙的质量分数.
(3)该稀盐酸的溶质质量分数.
15.今年中考化学技能考试中,小林抽到的考题是:用碳酸钠溶液来鉴别稀盐酸、食盐水和澄清石灰水.小林同学按以下过程进行作答:
【进行实验】
写出试管C中反应方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
【发现问题】如何处理上述废液才能减少对环境的污染?
【思考与分析】应先对废液中的溶质成分进行探究,后制定方案.
【实验与探究】
(1)小林将所有废液倒入一洁净烧杯中,静置后得到上层清液.
(2)取少量清液加入适量的氯化钙溶液(中性),再滴加几滴无色酚酞试液,若出现有白色沉淀且酚酞变红的现象,说明上层清液中一定有碳酸钠和氢氧化钠,一定没有Ca(OH)2、HCl.(填化学式)
【方法与应用】通过以上探究,处理上述废液的正确方法是:在废液中继续加入盐酸,调节溶液pH=7,蒸发获得氯化钠晶体.
【进行实验】
| 操作步骤 | 实验现象 | 实验结论 |
| 分别用A、B、C三支试管取样,然后各加入适量碳酸钠溶液 | A中无明显现象 B中有气体 C中有白色沉淀 | A中物质是食盐水 B中物质是稀盐酸 C中物质是澄清石灰水 |
【发现问题】如何处理上述废液才能减少对环境的污染?
【思考与分析】应先对废液中的溶质成分进行探究,后制定方案.
【实验与探究】
(1)小林将所有废液倒入一洁净烧杯中,静置后得到上层清液.
(2)取少量清液加入适量的氯化钙溶液(中性),再滴加几滴无色酚酞试液,若出现有白色沉淀且酚酞变红的现象,说明上层清液中一定有碳酸钠和氢氧化钠,一定没有Ca(OH)2、HCl.(填化学式)
【方法与应用】通过以上探究,处理上述废液的正确方法是:在废液中继续加入盐酸,调节溶液pH=7,蒸发获得氯化钠晶体.
5.下列叙述中,不正确的是( )
| A. | 硬水易生水垢 | |
| B. | 地球上可利用的淡水资源是有限的 | |
| C. | 软水与肥皂作用不易起泡沫 | |
| D. | 生活污水的任意排放会造成水体的污染 |
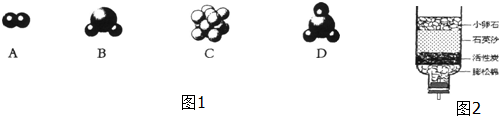
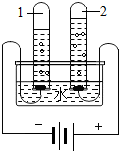 水和燃料都是宝贵的自然资源,需要珍视.请回答下列问题.
水和燃料都是宝贵的自然资源,需要珍视.请回答下列问题.